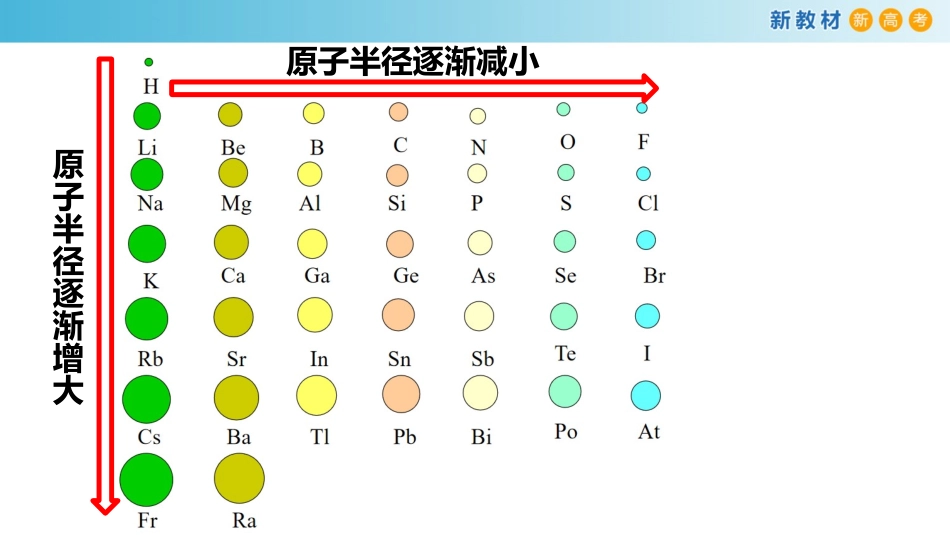
第四章·物质结构元素周期律第二节元素周期律第二课时原子半径逐渐增大原子半径逐渐减小【练习】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,原子半径按D、E、B、C、A顺序依次减小,B和E是同族,则下列推断中不正确的是:A.A、B、E一定不在同一周期B.A、D可能在同一主族C.C的最高氧化物的水化物可能显碱性D.C和D的单质可能化合成D2C2
BEDCA第一周期第二周期第三周期(H)C最小是第二周期第ⅢA族的B,其最高氧化物的水化物为酸,向右更应该是酸Na2O2C主族元素的化合价的规律有:1、同周期由左向右主族元素的最高正价逐渐有+1价升高至+7价(O和F一般不呈现正价)2、同主族元素的最高正价和最低负价相同(注意O和F)3、主族元素的最高正价等于该元素的原子最外层电子数,也等于其主族序数4、非金属元素的最高正价和最低负价的绝对值之和等于8(H的最低负价为-1)【练习】某主族元素R的最高正化合价与最低负化合价的代数和为4,下列有关叙述正确的是A、R一定是第四周期元素B、R的气态氢化物分子式为H2RC、R的气态氢化物比同周期其他元素的气态氢化物稳定D、R的气态氢化物的水溶液显碱性B【练习】五种短周期元素的原子半径、最高正化合价及负化合价见下表B下列叙述正确的是A.L的金属性比M的金属性弱B.Q、T两元素间可形成两性化合物C.T的单质是黄绿色气体D.L、R两元素的简单离子的核外电子数可能相等元素代号LMQRT原子半径/nm0
074化合价+2+2+3+6,-2-2根据元素化合价可以直接得到R为S,T为O;再根据原子半径和化合价得到L、M、Q分别为Mg、Be、AlAl2O3金属性增强非金属性减弱金属性减弱非金属性增强短周期主族元素金属性最强的元素是Na;非金属性最强的元素F
【思考与交流】根据之前的学习,总结比较元素的非金属性和金属