专题讲座化工流程题解题指导2下页末页上页首页一、无机化工流程题的特点3下页末页上页首页规律:主线主产品、分支副产品、回头为循环
核心考点:物质的分离操作、除杂试剂的选择、生产条件的控制
1.流程的呈现主要有以物质转化为主线,以操作过程为主线,甚至有时候会以设备为主线
这类题常围绕以下几个知识点进行设问:(1)反应速率与平衡理论的运用:反应物颗粒大小:反应速率、原料的利用率等,温度:反应速率、物质的稳定性、物质的结晶等;4下页末页上页首页(2)氧化还原反应的判断、化学方程式或离子方程式的书写;(3)利用控制pH分离除杂;(4)化学反应的能量变化;(5)实验基本操作:除杂、分离、检验、洗涤、干燥等;(6)流程中的物质转化和循环,资源的回收和利用;(7)环境保护与绿色化学评价
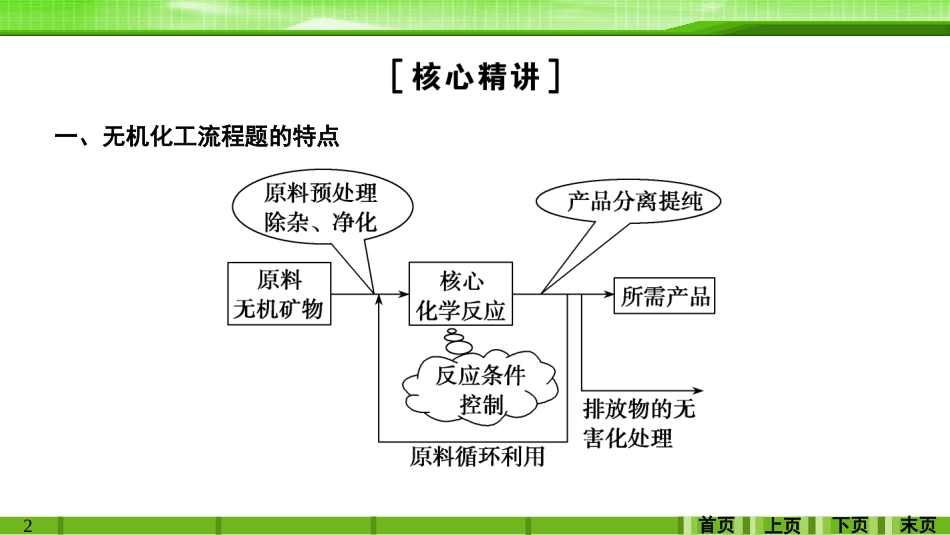
5下页末页上页首页二、无机化工流程题的结构工艺流程题的结构分题头、题干和题尾三部分
题头一般是简单介绍该工艺生产的原材料和工艺生产的目的(包括副产品);题干部分主要用框图形式将原料到产品的主要生产工艺流程表示出来;题尾主要是根据生产过程中涉及到的化学知识设置成一系列问题,构成一道完整的化学试题
题型特点:1.呈现形式:流程图、表格、图像
2.设问方式:措施、成分、物质、原因
6下页末页上页首页3.能力考查:获取信息的能力、分析问题的能力、迁移推理能力、表达能力
4.知识落点:基本理论、元素化合物、实验
无机工业流程题能够以真实的工业生产过程为背景,体现能力立意的命题指导思想,能够综合考查学生各方面的基础知识及将已有知识灵活应用在生产实际中解决问题的能力
三、解题思路明确整个流程及每一部分的目的→仔细分析每步发生的反应及得到的产物→结合基础理论与实际问题思考→注意答题的模式与要点
7下页末页上页首页1.在解这类题目时:首先,要粗读试题,尽量弄懂流程图,但不必将每一种物质都推出
其次,再精读试题,根据问题去