元素周期表(一)元素周期表(一)余二高邹丙铎Email:zbd2005@265
com看你学不学
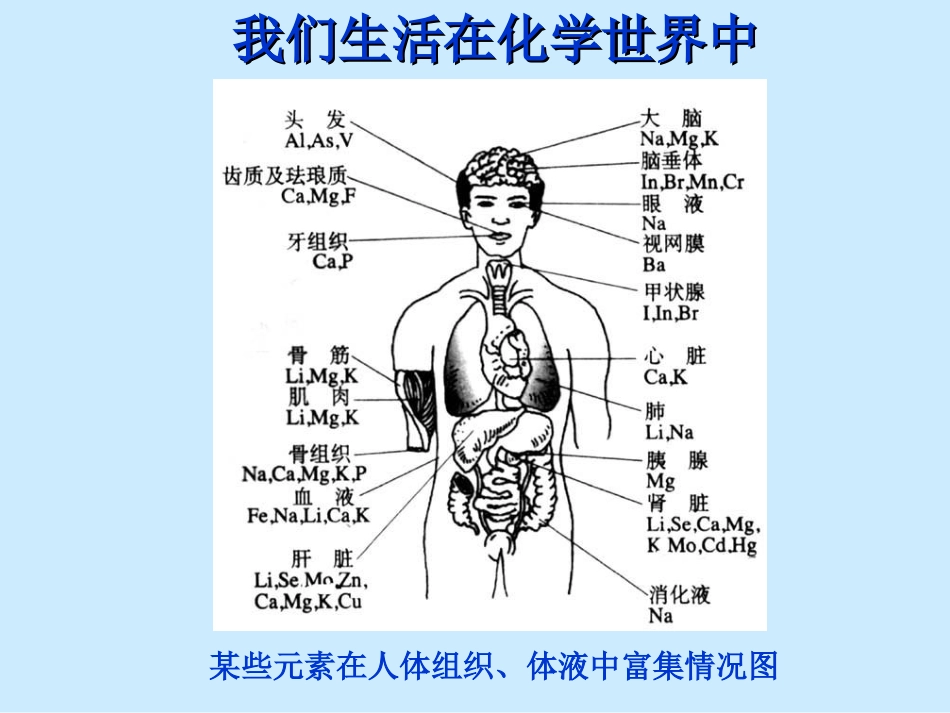
我们生活在化学世界中我们生活在化学世界中某些元素在人体组织、体液中富集情况图认识世界,必须认识化学元素认识世界,必须认识化学元素各种化学元素之间有何内在联系
——元素周期律
什么是元素周期律
——元素的性质随着元素原子序数的递增而呈现周期性的变化
包括:1、性质相似元素周期性出现2、原子结构周期性变化3、原子半径周期性变化4、元素化合价周期性变化想一想:考考你:你能否将1—18号元素编成一个小小的周期表
要求:1、将性质相似的元素归类
2、体现元素性质的周期性递变规律
编制原则:1、将最外层电子数相同的元素归为一列
2、将相同电子层数相同的元素排在一行
3、按原子序数的递增编排
Na11钠H1氢He2氦Li3锂Be4铍B5硼C6碳N7氮O8氧F9氟Ne10氖Mg12镁Al13铝Si14硅P15磷S16硫Cl17氯Ar18氩1~18元素周期表的参考结构☆元素周期表的发展历史☆元素周期表的发展历史Na11钠H1氢He2氦Li3锂Be4铍B5硼C6碳N7氮O8氧F9氟Ne10氖Mg12镁Al13铝Si14硅P15磷S16硫Cl17氯Ar18氩从18世纪中叶到19世纪中叶这100年间,随着生产和科学技术的发展,新的元素不断地被发现
到1869年人们已经发现了60多种元素,有原子量很小的氢,也有原子量很大的铀,并且积累了不少对这些元素的物理性质、化学性质的研究材料
究竟这些元素之间有没有内在的联系呢
人们在寻找元素性质之间的内在联系时提出了将元素进行分类的各种学说
1829年,德国耶那大学的化学教授德贝莱纳(DObereiner)根据元素性质的相似性,提出了“三素组”学说
但是,在当时已发现的54种元素中却只能把15种元素归入“三素组”
1865年,英国人纽兰兹(Newla