第四章物质结构元素周期律第二节元素周期律4
1元素性质的周期性变化规律同主族元素性质的规律:同主族元素,由上到下原子核外电子层数依次增加,原子半径逐渐增大,原子核对最外层电子的吸引逐渐减弱,原子失电子能力逐渐增强,得电子能力逐渐减弱,所以金属性逐渐增强,非金属性逐渐减弱
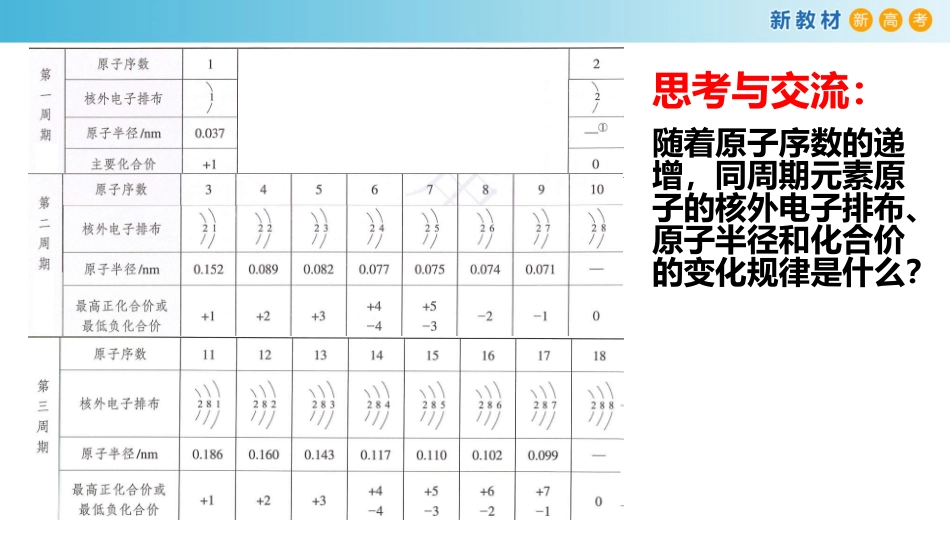
思考与交流:随着原子序数的递增,同周期元素原子的核外电子排布、原子半径和化合价的变化规律是什么
核外电子排布的规律:最外层电子数1→2最外层电子数1→8最外层电子数1→8同周期由左向右元素的原子最外层电子数从1逐渐增加,达到8电子的稳定结构
(K层为2电子的稳定结构)原子半径的变化规律:原子半径逐渐减小原子半径逐渐减小同周期由左向右元素的原子半径逐渐减小(不包括稀有气体)
原子半径逐渐增大原子半径逐渐减小半径最小的原子是什么
短周期主族元素中,原子半径最大的是哪种元素
NaH元素化合价的变化规律:正价:+1→+5,负价:-4→-1正价:+1→+7,负价:-4→-1同周期由左向右元素的最高正价逐渐升高(+1→+7,O和F无最高正价);元素的最低负价由ⅣA族的-4价逐渐升高至ⅦA族的-1价主要化合价的相关规律:最高正化合价=最外层电子数=主族序数最低负化合价的绝对值=8—最外层电子数随着原子序数的递增原子的核外电子排布原子半径化合价呈现周期性的变化元素的金属性和非金属性是否也随原子序数的变化呈现周期性变化呢
证明金属性强弱的方法有:1、单质与水(或酸)反应生成氢气的难易(金属性越强反应越容易)2、最高价氧化物的水化物——氢氧化物的碱性强弱(金属性越强氢氧化物的碱性越强)证明非金属性强弱的方法有:1、单质与氢气反应生成气态氢化物的难易(非金属性越强反应越容易)2、最高价氧化物的水化物的酸性强弱(非金属性越强酸性越强)3、气态氢化物的稳定性(非金属性越强气态氢化物越稳定)实验探究:第三周期元素性质的递变演示实验