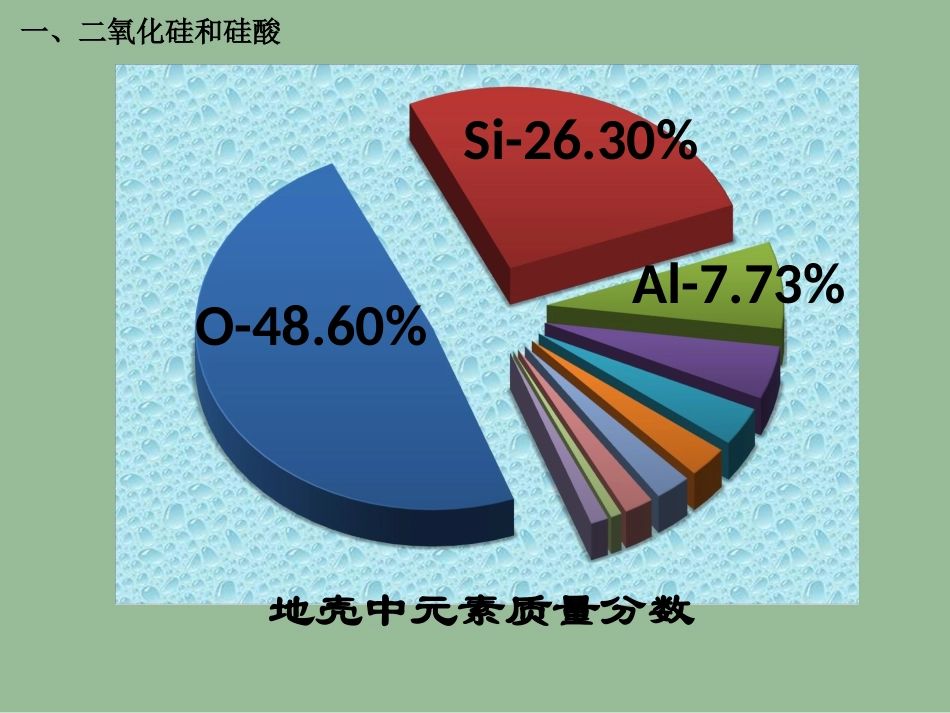
第四章非金属及其化合物第一节无机非金属材料的主角—硅第1课时新课标人教版高中化学课件系列必修化学1Al-7
73%O-48
60%Si-26
30%地壳中元素质量分数一、二氧化硅和硅酸一、二氧化硅和硅酸一、二氧化硅和硅酸长石一、二氧化硅和硅酸一、二氧化硅和硅酸滑石一、二氧化硅和硅酸石棉一、二氧化硅和硅酸高岭土一、二氧化硅和硅酸粘土一、二氧化硅和硅酸画出硅的原子结构示意图分析:既不易失电子,又不易得电子,主要形成四价的化合物
硅元素与哪种原子的结构相似
碳一、二氧化硅和硅酸你知道吗
常温下,单质碳、硅的化学性质都不活泼,为什么碳在自然界中有稳定的单质(金刚石)存在,而硅却没有
单质硅的化学性质虽然稳定,但硅是一种亲氧元素,硅原子和氧原子的结合非常牢固,形成的二氧化硅或硅酸盐中的硅氧化学键非常牢固,硅氧键一旦形成就很难被破坏,所以,自然界中硅都是以二氧化硅或硅酸盐的形式存在,没有游离态的硅
硅是一种亲氧元素,在自然界中主要以氧化物及硅酸盐的形式存在
一、二氧化硅和硅酸(1)存在硅石(12%)结晶形:石英无定形水晶玛瑙1、二氧化硅一、二氧化硅和硅酸石英水晶一、二氧化硅和硅酸茶水晶紫水晶蔷薇石英黄水晶一、二氧化硅和硅酸玛瑙一、二氧化硅和硅酸一、二氧化硅和硅酸一、二氧化硅和硅酸一、二氧化硅和硅酸光导纤维光缆一、二氧化硅和硅酸(2)用途:光导纤维石英:耐高温化学仪器、石英电子表、石英钟水晶:电子工业的重要部件、光学仪器、高级工艺品和眼镜片玛瑙:精密仪器轴承、耐磨器皿和装饰品光纤视频玛瑙饰品一、二氧化硅和硅酸物理性质:_____________________________化学稳定性:_________________________通常条件下,很稳定硬度大、熔点高、难溶于水一、二氧化硅和硅酸思考为什么二氧化硅和二氧化碳物理性质有这么大的差别
是结构上的不同科学视野P74一、二氧化硅和