第七章电化学基础真题实战11
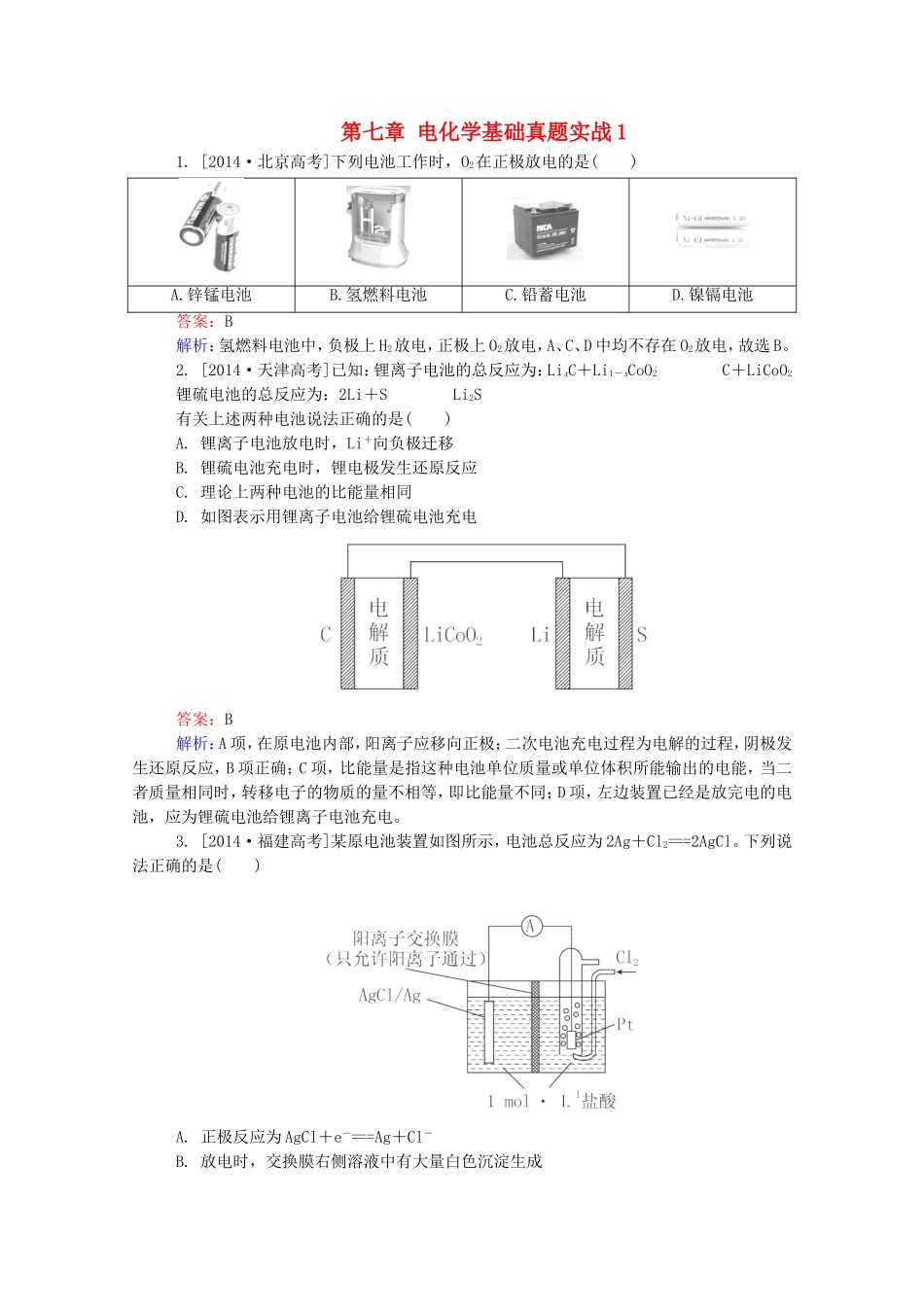
[2014·北京高考]下列电池工作时,O2在正极放电的是()A
氢燃料电池C
镍镉电池答案:B解析:氢燃料电池中,负极上H2放电,正极上O2放电,A、C、D中均不存在O2放电,故选B
[2014·天津高考]已知:锂离子电池的总反应为:LixC+Li1-xCoO2C+LiCoO2锂硫电池的总反应为:2Li+SLi2S有关上述两种电池说法正确的是()A
锂离子电池放电时,Li+向负极迁移B
锂硫电池充电时,锂电极发生还原反应C
理论上两种电池的比能量相同D
如图表示用锂离子电池给锂硫电池充电答案:B解析:A项,在原电池内部,阳离子应移向正极;二次电池充电过程为电解的过程,阴极发生还原反应,B项正确;C项,比能量是指这种电池单位质量或单位体积所能输出的电能,当二者质量相同时,转移电子的物质的量不相等,即比能量不同;D项,左边装置已经是放完电的电池,应为锂硫电池给锂离子电池充电
[2014·福建高考]某原电池装置如图所示,电池总反应为2Ag+Cl2===2AgCl
下列说法正确的是()A
正极反应为AgCl+e-===Ag+Cl-B
放电时,交换膜右侧溶液中有大量白色沉淀生成C
若用NaCl溶液代替盐酸,则电池总反应随之改变D
当电路中转移0
01mole-时,交换膜左侧溶液中约减少0
02mol离子答案:D解析:在原电池中负极发生氧化反应,正极发生还原反应,故由总反应式可知,负极反应为:2Ag-2e-+2Cl-===2AgCl,正极反应为:Cl2+2e-===2Cl-,A项错误;由于电解质溶液中含有大量Cl-,故放电时,Ag+在交换膜左侧即与Cl-反应生成AgCl沉淀,B项错误;用NaCl溶液代替盐酸,电池总反应不变,C项错误;电路中转移0
01mole-时,交换膜左侧溶液有0
01molCl-参与反应