化学平衡的移动讲义※回顾请你说出浓度、压强、温度、催化剂等外界条件对化学反应速率的影响1
催化剂一、化学平衡的移动原因结果化学平衡的移动1、定义:已达到平衡状态的可逆反应,反应条件改变时,平衡混合物里各组成物质的百分含量也就会改变而达到新的平衡状态叫化学平衡移动
即旧的化学平衡被破坏、新的化学平衡建立的过程就是平衡移动
2、原因:二、影响化学平衡移动的因素1、浓度的变化对化学平衡的影响H+浓度对平衡:Cr2O72-+H2O2CrO42-+2H+的影响橙色黄色实验现象结论①K2Cr2O7溶液中,滴加数滴NaOH溶液将①溶液分成两份,一份滴加HNO3溶液,另一份作对比规律:其它条件不变的情况下①增大反应物浓度或减小生成物浓度平衡向移动②增大生成物浓度或减小反应物浓度平衡向移动原因:Cr2O72-+H2O2CrO42-+2H+Qc=,加入NaOH溶液,C(H+),QcK,此时V(正)V(逆),平衡向移动,使Qc至与K相等而达到新的平衡状态,溶液变为色
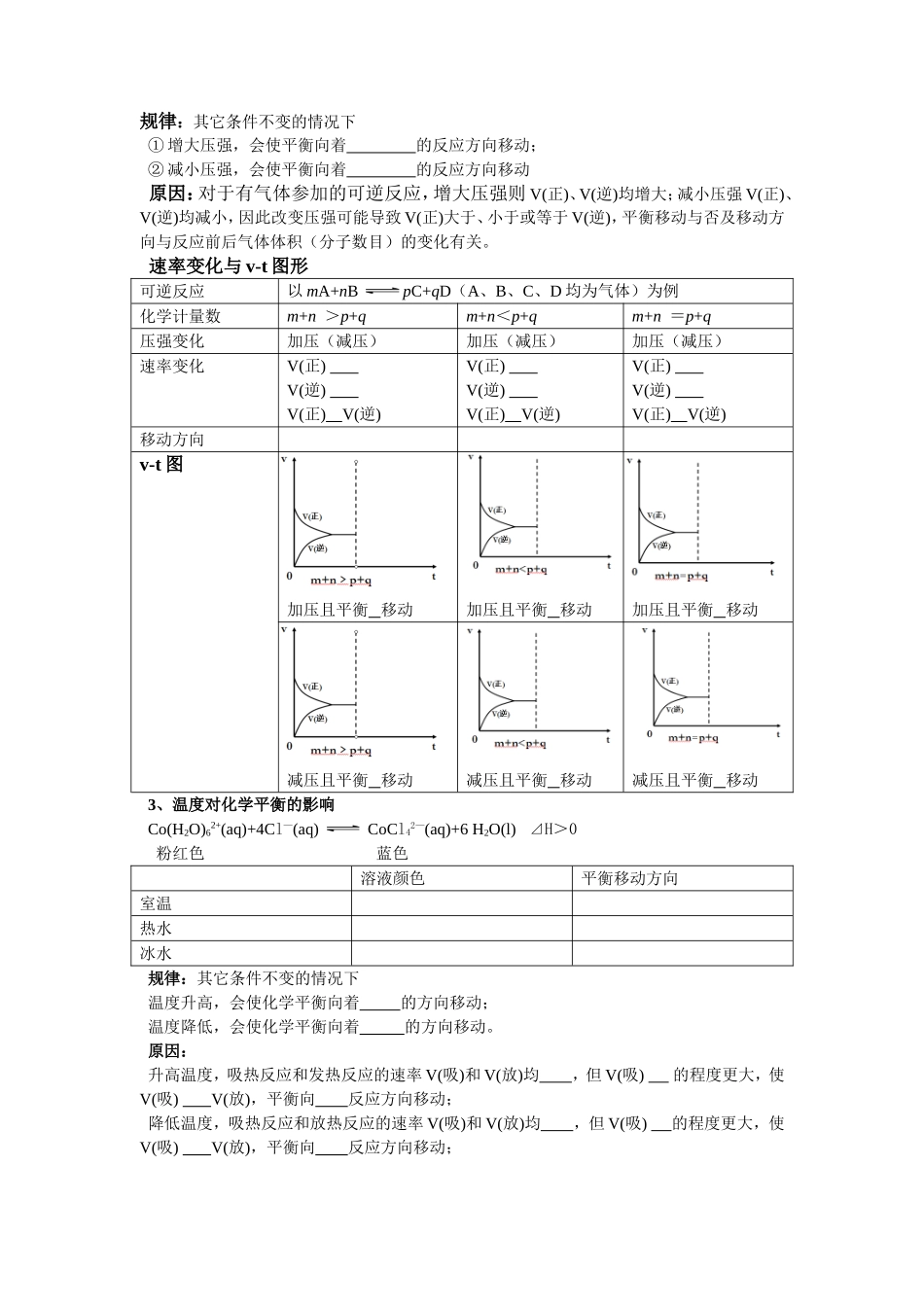
速率变化与v-t图形化学平衡aA+bBcC+dD(A、B、C、D为非固体、非纯液体)浓度变化增大反应物浓度增大生成物浓度减小反应物浓度减小生成物浓度速率变化V(正)V(逆)V(正)V(逆)V(正)V(逆)V(正)V(逆)V(正)V(逆)V(正)V(逆)V(正)V(逆)V(正)V(逆)平衡移动方向v-t图2、压强对化学平衡的影响改变条件平衡被破坏V’(正)≠V’(逆)化学平衡V(正)=V(逆)又达到新平衡V”(正)=V”(逆)一定时间后规律:其它条件不变的情况下①增大压强,会使平衡向着的反应方向移动;②减小压强,会使平衡向着的反应方向移动原因:对于有气体参加的可逆反应,增大压强则V(正)、V(逆)均增大;减小压强V(正)、V(逆)均减小,因此改变压强可能导致V(正)大于、小于或等于V(逆),平衡移动与否及移动方