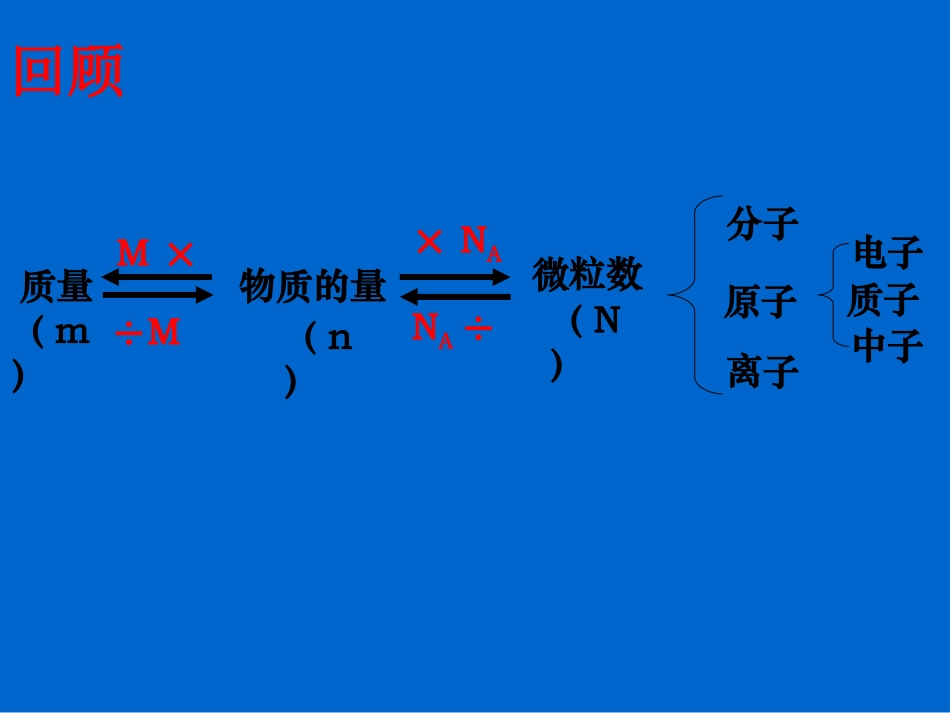
÷MM××NANA÷质量(m)物质的量(n)分子离子电子原子质子中子微粒数(N)回顾一、物质的聚集状态1、物质的聚集状态主要有三种:气态、液态和固态为什么固态,液态和气态物质的某些性质存在差异?这与物质的微观结构有何联系?思考:FePbH2OH2SO4气体分子物质的聚集状态微观结构微粒的运动方式宏观性质固态液态气态微粒排列紧密,微粒间空隙很小微粒排列较紧密,微粒间空隙较小微粒之间的距离较大在固定的位置上振动可以自由移动可以自由移动有固定的形状,几乎不能被压缩没有固定的形状,但不易被压缩没有固定的形状,且容易被压缩1mol任何微粒的集合体所含的微粒的数目都相同,1mol微粒的质量通常不同。1mol物质的体积是否相同?交流与讨论交流与讨论物质摩尔质量/g.mol-1密度1mol物质的体积Al26.982.70g.cm-3Fe55.857.86g.cm-3H2O18.020.998g.cm-3C2H5OH46.070.789g.cm-3H22.0160.0899g.L-1N228.021.25g.L-1CO28.011.25g.L-19.99cm37.11cm318.1cm358.4cm322.4L22.4L22.4L3.1mol的固体和液体的体积较小,1mol气体的体积较大。1.1mol不同的固态或液态的物质,体积不同。2.在相同状况下,1mol气体的体积基本相同。[结论]1、为什么固体或液体的体积较小,而气体较大?2、为什么在相同状况下1mol固体或液体的体积不相同?1mol气体的体积相同?3、物质体积即物质所占据空间的大小取决于哪些微观因素?4、不同状态的物质体积主要取决于什么因素?5、从微观角度看,温度和压强的改变会引起气体分子怎样的变化?1、在温度压强一定的情况下决定物质体积大小的因素有三个:①微粒的数目②微粒的大小③微粒之间的距离二、影响物质体积大小的因素影响物质体积大小的主要因素微粒的数目微粒的大小微粒的间距固、液态气态√√√√[结论1]任何1mol固体物质或液体物质所含的微粒的数目相同,微粒之间的距离很小,但微粒的大小不同,所以1mol固体物质或液体物质的体积往往是不同的。在温度、压强一定时,相同分子数目的气体体积大小主要决定于气体分子之间的距离,而不是分子本身体积的大小。[结论2]三、气体摩尔体积1、定义:单位物质的量的气体所占的体积。2、符号:Vm4、表达式:3、单位:L·mol-1mVnVmVVnVm=vn约定特例:在标准状况(273K,101kPa)下,1mol任何气体所占的体积都约为22.4L(或气体在标准状况下的摩尔体积约是22.4L·mol-1)。22.4L几点注意:1、状况:标准状况(0,1atm).℃指某个一定温度和压强下2、定量:1mol3、数值:约为22.4L4、对象:任何气体(气体体积与微粒数目有关,与种类无关。)5、单位:升/摩6、有关计算:(标准状况下)V=n×22.4L/mol(n---气体的物质的量)在温度、压强一定时,任何具有相同微粒数的气体都具有大致相同的体积。即同温、同压下,相同体积的任何气体都具有大致相同的分子数。————阿伏加德罗定律阿伏加德罗定律[引入]1.标准状况下,1mol任何物质的体积都约是22.4L。(错,物质应是气体)2.标准状况下,1molO2和N2混合气体的体积约为22.4L。(对,气体体积与分子种类无关)判断[练习]3.22.4L气体所含分子数一定大于11.2L气体所含的分子数。(错,未指明气体体积是否在相同条件下测定)4.标准状况下,气体的摩尔体积都是22.4L。(错,“约为”;单位应为L.mol-1)5.只有在标准状况下,气体的摩尔体积才可能约为22.4L.mol-1。(错,不一定)ρρ[练习](1)标况下,22.4升CO2是多少摩?(2)标况下,0.2摩O2和0.8摩CO2,求气体体积?(3)1atm,14℃时1摩气体与标况时比体积如何?(4)同一条件下100mlH2和多大体积Cl2恰好完全反应,生成多少体积氯化氢气体?Zn+2HCl===ZnCl2+H2↑答:最多可收集到4.48L(标准状况)氢气。0.200molV(H2)22.4L1mol[练习]13.0克锌与足量的稀盐酸完全反应,最多可收集到多少体积(标准状况)的氢气?V(H2)==0.200mol×22.4L1mol==4.48L解:13.0克锌的物质的量为0.200mol拓展视野晶体非晶态物质微粒排列外形熔点物质类型规则无规则规则几何外形无规则几何外形固定熔点(mp.)无固定熔点金属/氯化钠纯碱/冰/干冰石蜡/玻璃/水泥ρρ×Vm气体体积V(标况)质量物质的量粒子数÷M×M×NA÷NAmnN小结有关气体各物理量的计算关系÷Vm