第四章电化学基础考点聚焦1
理解原电池原理,熟记金属活动顺序,了解化学腐蚀与电化学腐蚀及一般防腐方法;2
了解电解和电镀的基本原理及应用
主要内容回扣1、原电池、电解池、电镀池判定规律若无外接电源,可能是原电池,然后依据原电池的形成条件分析判定,主要思路是“三看”
先看电极:两极为导体且活泼性不同;再看溶液:两极插入电解质溶液中后看回路:形成闭合回路或两极接触
若有外接电源,两极插入电解质溶液中,则可能是电解池或电镀池
当阳极金属与电解质溶液中的金属阳离子相同则为电镀池,其余情况为电解池
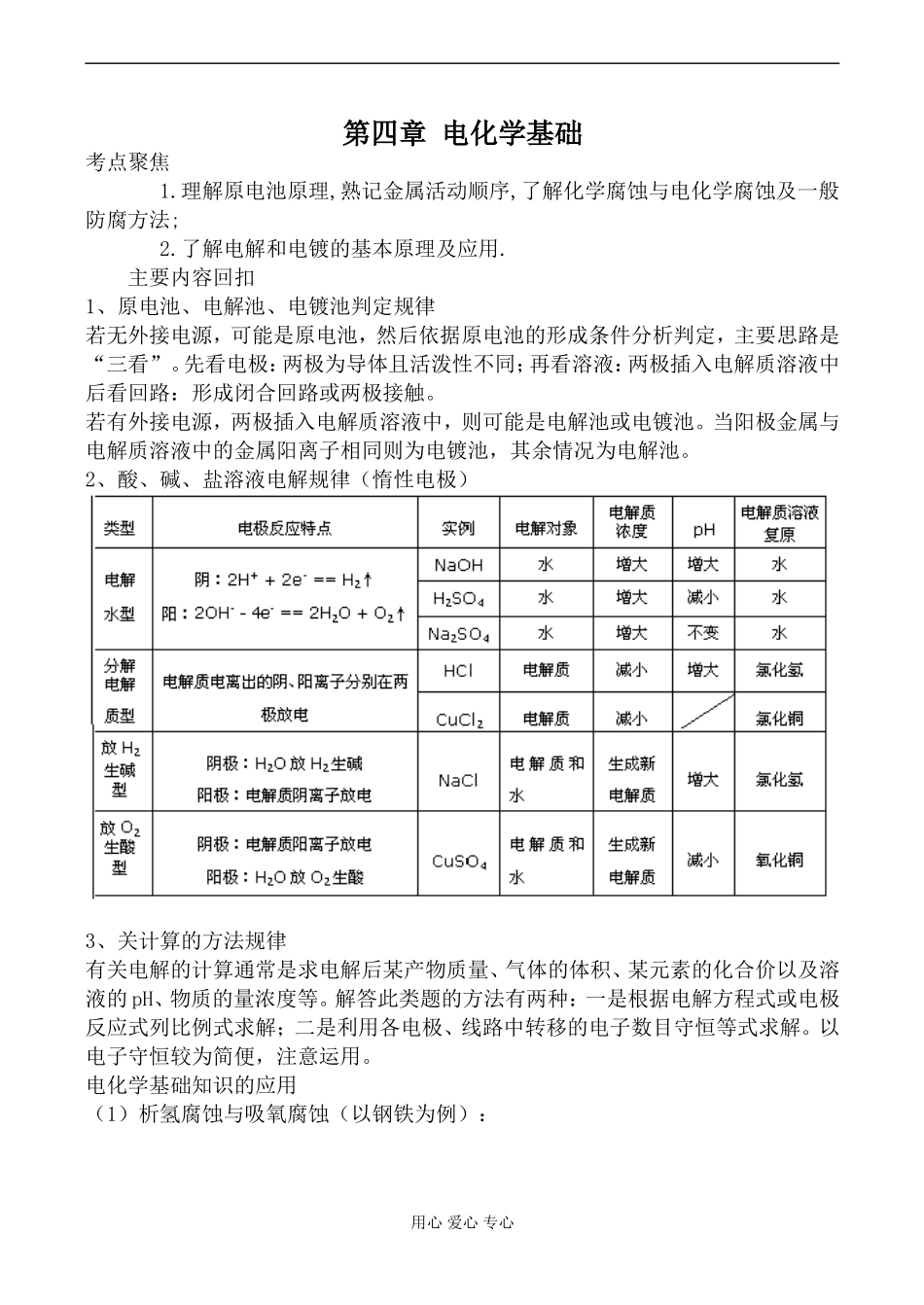
2、酸、碱、盐溶液电解规律(惰性电极)3、关计算的方法规律有关电解的计算通常是求电解后某产物质量、气体的体积、某元素的化合价以及溶液的pH、物质的量浓度等
解答此类题的方法有两种:一是根据电解方程式或电极反应式列比例式求解;二是利用各电极、线路中转移的电子数目守恒等式求解
以电子守恒较为简便,注意运用
电化学基础知识的应用(1)析氢腐蚀与吸氧腐蚀(以钢铁为例):用心爱心专心(2)的防护,主要有下面几种情况:改变金属的内部结构,例如把Ni、Cr等加入普通钢里制成不锈钢;覆盖保护层,例如涂油层、油漆、搪瓷、熟料等,另外还有电镀耐腐蚀的金属(Zn、Sn、Cr、Ni等);电化学保护法,多采用牺牲阳极保护法,如在船只的螺旋桨附近的船体上镶嵌活泼金属锌块,另外可采用与电源负极相连接的保护方法,例如大型水坝船闸的保护就是让铁闸门和电源负极相连
(3)电解原理的应用氯碱工业(电解饱和食盐水):2NaCl+2H2O电解==2NaOH+H2↑+Cl2↑;活泼金属Na、Mg、Al的制取,例如,电解熔融的NaOH制金属Na,4NaOH电解==4Na+2H2O+O2↑(其中Na为阴极区产物而H2O和O2则为阳极区产物);金属的精炼,例如铜的精炼,以粗铜为阳极,精铜为阴极,含铜离子的溶液作电解质溶液;电镀,待镀金属制