专题1课题3硝酸钾晶体的制备问题问题11、工业上多以硝酸钠和氯、工业上多以硝酸钠和氯化钾为主要原料生产硝酸钾,副化钾为主要原料生产硝酸钾,副产品为氯化钠
反应方程为产品为氯化钠
反应方程为NaNONaNO33+KCl=NaCl+KNO+KCl=NaCl+KNO33①①该反应的原理是什么
该反应的原理是什么
②②如何分离硝酸钾和氯化钠的混如何分离硝酸钾和氯化钠的混合物
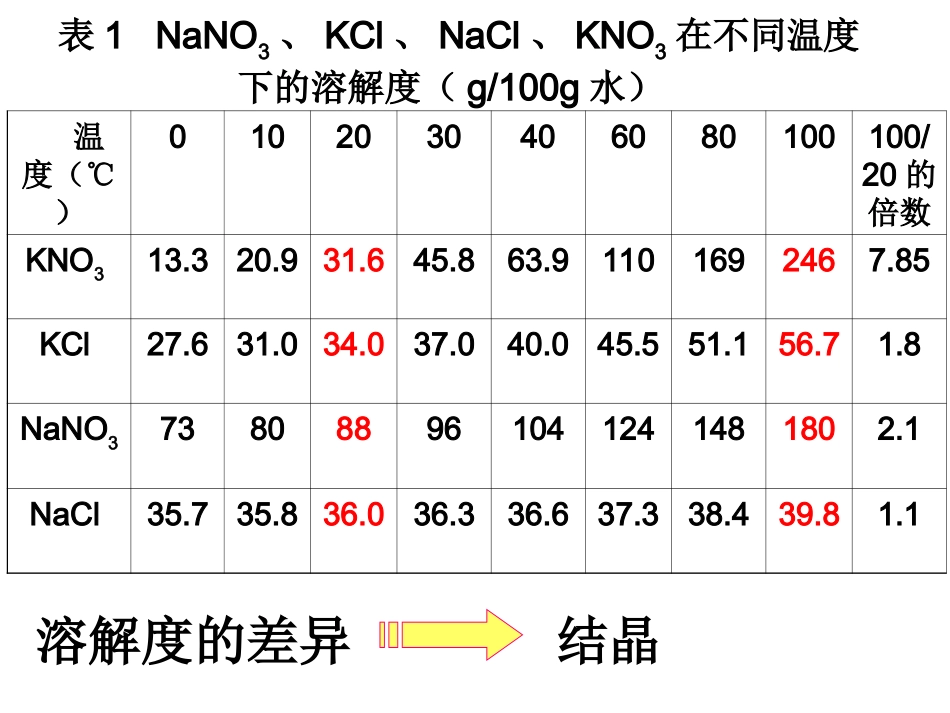
表1NaNO3、KCl、NaCl、KNO3在不同温度下的溶解度(g/100g水)温度(℃)0102030406080100100/20的倍数KNO313
91101692467
85KCl27
8NaNO3738088961041241481802
1NaCl35
1溶解度的差异结晶在较高温度下,达到饱和的NaCl先结晶分离;然后,在低温下,KNO3达饱和,得到产品
蒸发溶解热过滤结晶一、实验操作要点热过滤:趁热过滤,得KNO3饱和溶液(回收NaCl晶体)结晶:KNO3溶液冷却有KNO3晶体析出蒸发:小火加热至有较多晶体析出[2]溶解:20gNaNO317gKCl35ml水[1]抽滤:得KNO3晶体,用少量饱和KNO3溶液淋洗晶体称量:称量得,粗KNO3质量[2]“溶液体积蒸发至原来的一半”改为“蒸发至溶液体积约为40mL”[1]此时溶液体积约为50mL(1)制备KNO3粗品减压过滤(也称抽滤或吸滤)阅读P14:操作向导(注意点)快速得到较干燥的沉淀过滤抽滤比较过滤与比较过滤与抽滤的区别抽滤的区别问题问题22、这样得到的晶体是否、这样得到的晶体是否纯净
若不纯,应如何提纯
若不纯,应如何提纯
第一次结晶得到的晶体纯第一次结晶得到的晶体纯度不合要求