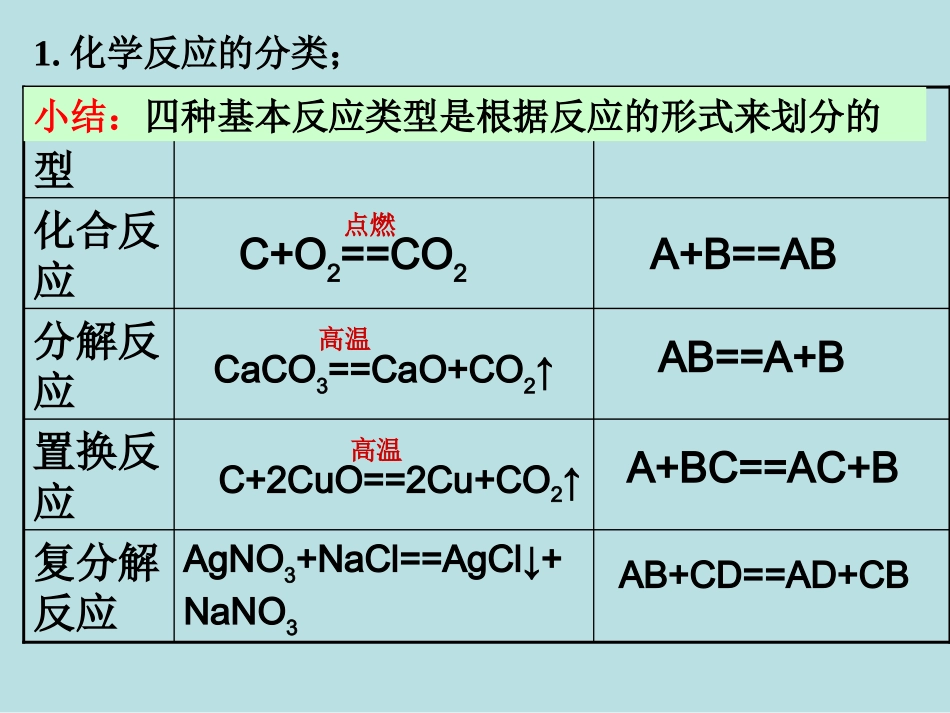
第二章化学物质及其变化第三节氧化还原反应1AB+CD==AD+CBAgNO3+NaCl==AgCl↓+NaNO3复分解反应A+BC==AC+B高温C+2CuO==2Cu+CO2↑置换反应AB==A+B高温CaCO3==CaO+CO2↑分解反应A+B==AB点燃C+O2==CO2化合反应表示式举例反应类型1
化学反应的分类;小结:四种基本反应类型是根据反应的形式来划分的1、Fe2O3+3CO====2Fe+3CO2属于四大基本反应类型中的哪一种
高温得到氧,被氧化失去氧,被还原Fe2O3+3CO====2Fe+3CO2高温思考·交流2、请从氧化反应和还原反应角度分析Fe2O3+3CO====2Fe+3CO2属于那种反应类型
氧化反应和还原反应是分别独立进行的吗
氧化反应和还原反应总是同时进行的一、氧化还原反应一、氧化还原反应1、从得氧、失氧分析CuO+H2===Cu+H2O△得到氧,被氧化失去氧,被还原氧化还原反应同时发生,不可分割
物质得到氧被氧化,发生氧化反应
物质失去氧被还原,发生还原反应
第三节氧化还原反应第三节氧化还原反应3、标出下列氧化还原反应中的各个元素的化合价,观察化合价有无变化,变化有无规律
C+2CuO===CO2↑+2Cu高温C+H2O====CO+H2高温还原反应,化合价降低+100+2+200+4氧化反应,化合价升高氧化反应,化合价升高还原反应,化合价降低思考·交流4、氧化还原反应是否一定存在得失氧
请分析下面的反应
化合价升高被氧化被还原化合价降低2Na+Cl2====2NaCl点燃思考·交流2、从化合价升降分析氧化还原反应:有元素化合价升降的化学反应
(表观特征)氧化反应:物质所含元素化合价升高的反应
还原反应:物质所含元素化合价降低的反应
氧化还原反应的判断依据是:有无化合价的升降化合价升高→被氧化→氧化反应化合价降低→被还原→还原反应