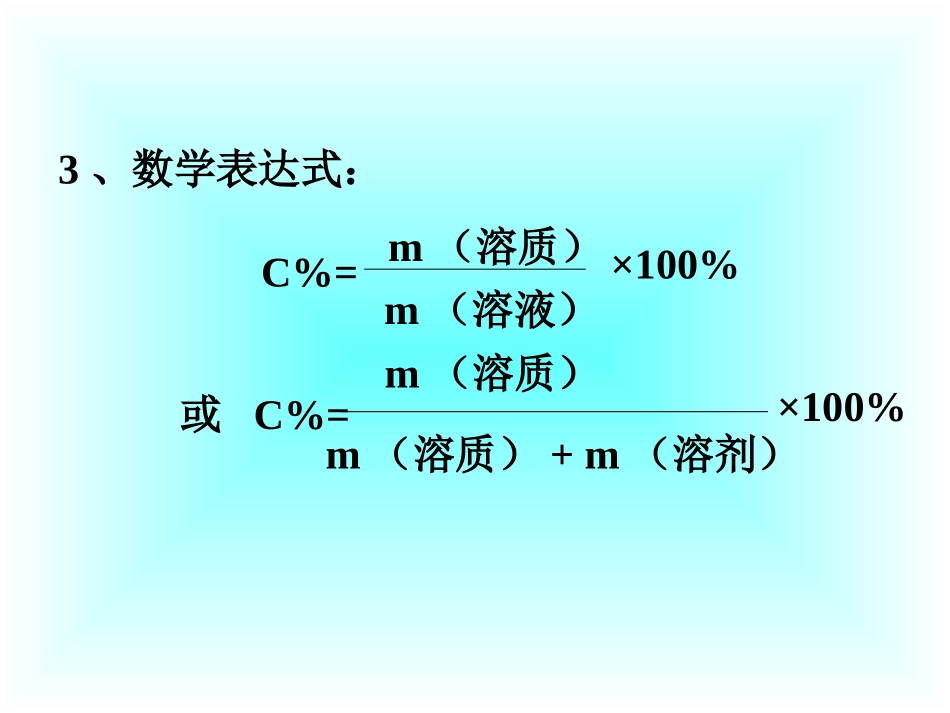
7、3溶液浓稀的表示溶质质量分数=溶质质量溶液质量×100%或=溶质质量溶质质量+溶剂质量×100%一、溶液中溶质质量分数(质量比)1、定义:是指溶液中溶质的质量与溶液的质量之比
表示意义:表示一定量溶液中含有溶质的多少2、表示方法:溶质质量=溶液质量×溶质质量分数3、数学表达式:m(溶质)C%=m(溶液)×100%或C%=m(溶质)m(溶质)+m(溶剂)×100%二、有关C%的计算食盐溶液水NaCl固体浓度100克96克
3%4克4%190克5%24克126克135
7克100克操作措施溶质质量溶剂质量溶液质量浓度去掉一部分加水加入溶质减少溶质蒸去水减少减少减少不变不变增加增加减小不变减少减少增加不变增加增大减少不变减少减小增大每份溶液作不同操作的情况分析练习1、将5克氯化钠完全溶解在45克水中,计算该溶液的浓度
2、配制80克20%的硝酸钾溶液,需硝酸钾和水各多少克
解:m(硝酸钾)=80克×20%=16克m(水)=80克-16克=64克答:配制80克20%的硝酸钾溶液需硝酸钾16克和水64克
3、判断下列说法是否正确,并加以改正
⑴在100克水中溶解30克食盐,溶液的百分比浓度是30%
⑵在90克水里溶解10克食盐,溶液的百分比浓度是10%
⑶从100克10%的食盐溶液里取出10克,其浓度是10%
⑷将100克10%的食盐溶液和200克10%的食盐溶液混合,混合溶液的浓度是20%⑸20℃时,100克水中最多溶解36克食盐,它的溶解度是36克,浓度是36%
(×)(√)(√)(×)(×)三、溶解度(S)与质量浓度(C%)的换算1、联系:饱和溶液浓度=S100+S×100%2、不同点:条件状态溶剂计算式单位SC%一定温度下常温饱和不一定100克不一定S=m溶质m溶剂×100克C%=m溶质m溶液×100%克无练习1、