实验化学复习一、从海带中提取碘的实验方案(1)称取3g干海带,用刷子把干海带表面的附着物刷净(不要用水洗,有I-)
将海带剪碎,用酒精润湿(便于灼烧)后,放在坩埚中
(2)用酒精灯灼烧盛有海带的坩埚,至海带完全成灰,停止加热,冷却
(3)将海带灰转移到小烧杯中,再向烧杯中加入10ml蒸馏水,搅拌,煮沸2min-3min,使可溶物溶解,过滤
(4)向滤液中滴入几滴稀硫酸,再加入约1mlH2O2溶液,观察现象
(5)取少量上述滤液,加几滴淀粉溶液,观察现象
(6)取剩余上述滤液于分液漏斗,加入约5ml煤油萃取实验注意事项实验方法海带不要用水洗,以免洗去海带中的碘;用干海带从而易于燃烧;灼烧海带的地方要注意通风
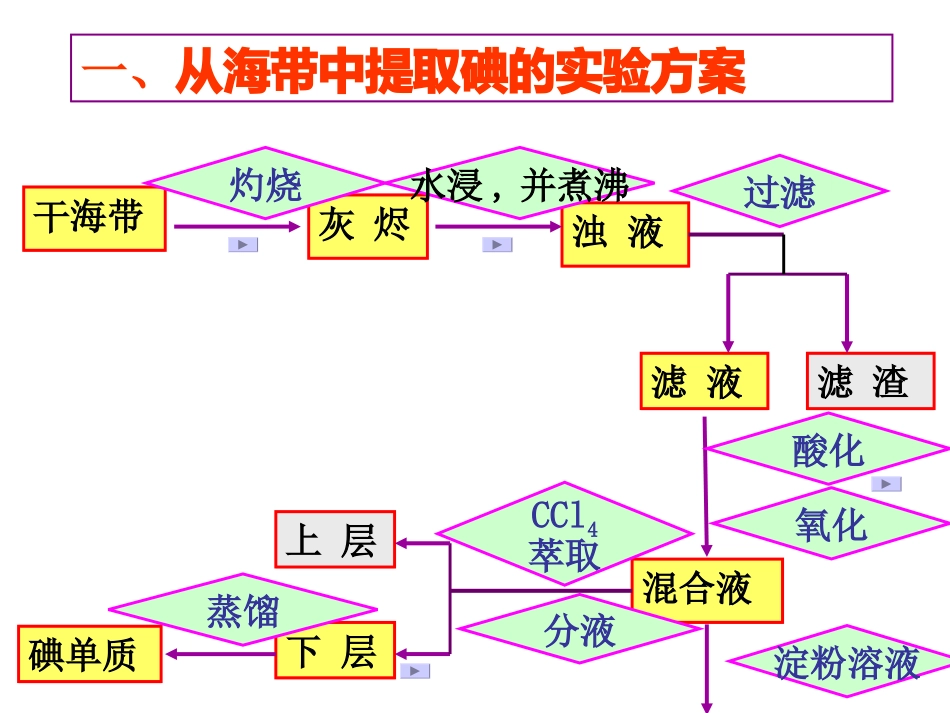
干海带灰烬浊液滤液混合液上层下层碘单质灼烧滤渣一、从海带中提取碘的实验方案水浸,并煮沸过滤酸化CCl4萃取分液蒸馏氧化淀粉溶液1
灼烧的作用是什么
思考与交流将干海带高温灼烧,使有机物转化为CO2和H2O,呈气态逸散
坩埚、坩埚钳、三角架、泥三角、酒精灯2
灼烧海带时用到哪些仪器
注意热坩埚不能放在桌面上
水浸时常常要将悬浊液煮沸2~3min,目的是什么
思考与交流加快碘化物在水中的溶解,以使灰烬中的I-尽可能多的进入溶液
酸化作用是什么
思考与交流海带灰的浸出液中含有碳酸钠(碳酸钾)等使溶液显碱性的物质,酸化的目的是使溶液呈弱酸性,有利于氧化剂把I-氧化为I2
你认为最好选用哪种氧化剂
思考与交流问3氧化2I-+H2O2+2H+=I2+2H2O2I-+Cl2=2Cl-+I2注意:若氯水过量,则Cl2能进一步将碘单质氧化
I-+3Cl2+3H2O=6Cl-+IO3-+6H+思考:若用碘盐中的KIO3作氧化剂,在酸性溶液中氧化I-,写出反应的离子方程式
5I-+IO3-+6H+=3I2+3H2O氯水、双氧水等•若要分离碘的CCl4溶液,分别得到碘和CCl4,