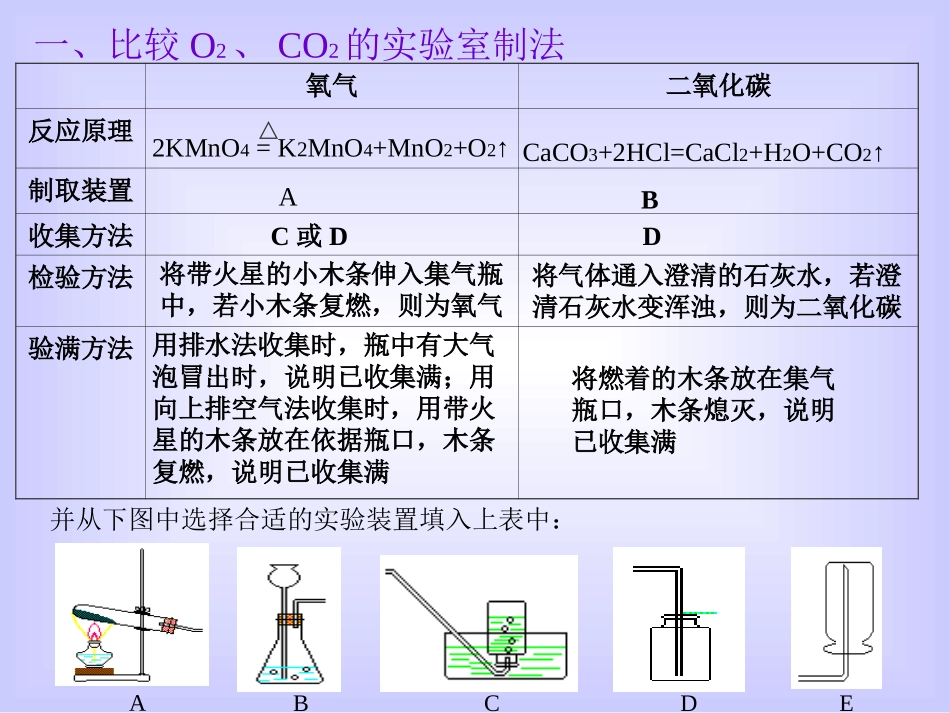
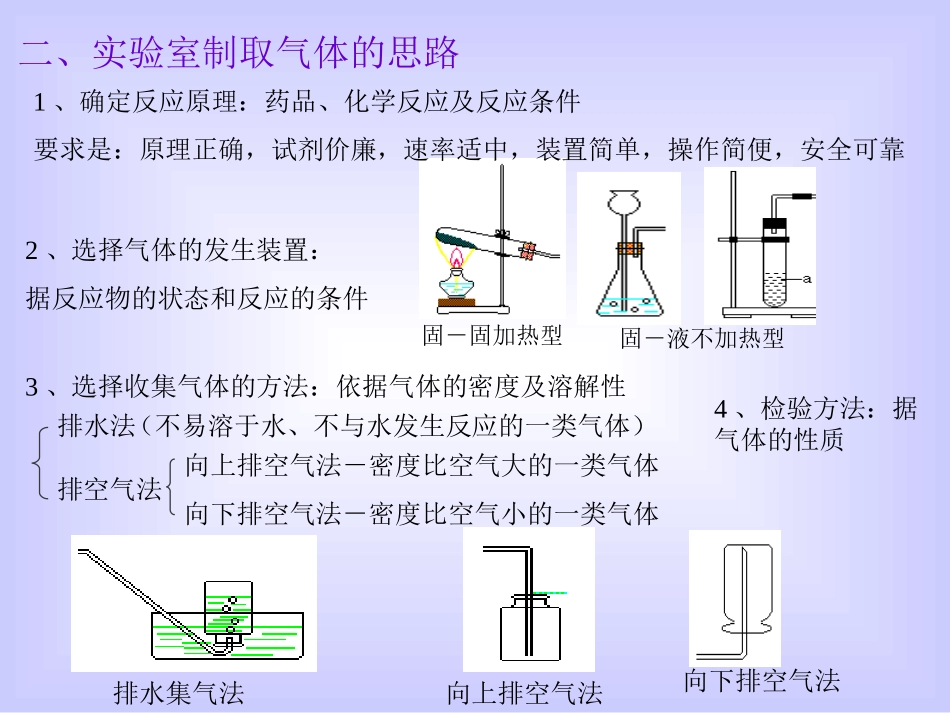
一、比较O2、CO2的实验室制法氧气二氧化碳反应原理制取装置收集方法检验方法验满方法2KMnO4=K2MnO4+MnO2+O2↑CaCO3+2HCl=CaCl2+H2O+CO2↑并从下图中选择合适的实验装置填入上表中:ABCDEAC或DDB将带火星的小木条伸入集气瓶中,若小木条复燃,则为氧气将气体通入澄清的石灰水,若澄清石灰水变浑浊,则为二氧化碳用排水法收集时,瓶中有大气泡冒出时,说明已收集满;用向上排空气法收集时,用带火星的木条放在依据瓶口,木条复燃,说明已收集满将燃着的木条放在集气瓶口,木条熄灭,说明已收集满固-固加热型固-液不加热型1、确定反应原理:药品、化学反应及反应条件要求是:原理正确,试剂价廉,速率适中,装置简单,操作简便,安全可靠2、选择气体的发生装置:据反应物的状态和反应的条件二、实验室制取气体的思路排水集气法3、选择收集气体的方法:依据气体的密度及溶解性向上排空气法向下排空气法排水法排空气法向上排空气法-密度比空气大的一类气体向下排空气法-密度比空气小的一类气体(不易溶于水、不与水发生反应的一类气体)4、检验方法:据气体的性质ABCDE想一想根据下图所示实验装置回答下列问题
1、A装置试管口略向下倾斜是为了防止试管:B装置中长颈漏斗末端应伸入液面下,目的是;伸进D、E中的导管均应接近集气瓶的底部,是为了
炸裂防止气体从长颈漏斗中逸出排尽瓶中的空气2、氨气在通常情况下是一促无色有刺激性气味的气体,密度比空气小,极易溶于水
实验室常用加热氯化氨和熟石灰两种固体的混合物制取氨气
(1)写出实验室制取氨气的化学方程式:
(2)实验室制取氨气的装置,可选用,收集氨气可用
(填序号)2NH4CL+Ca(OH)2=CaCl2+2NH3↑+2H2OAE动动脑右图是制备二氧化碳的装置图
该装置的特点是:打开弹簧夹,大理石和盐酸接触,发生反应,关闭弹簧夹后,盐酸被反应产生的二