第二章分子结构与性质主要知识点复习S-S重叠S-P重叠P-P重叠1
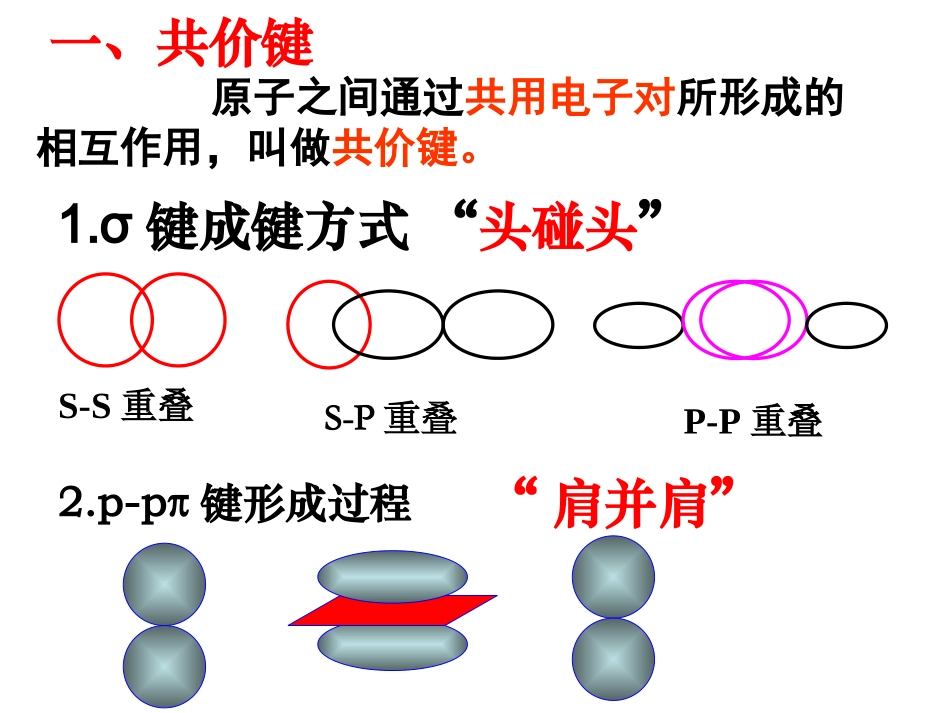
σ键成键方式“头碰头”一、共价键原子之间通过共用电子对所形成的相互作用,叫做共价键
p-pπ键形成过程“肩并肩”二、键参数1
键能气态基态原子形成1mol共价键释放的最低能量(或拆开1mol共价键所吸收的能量),例如H-H键的键能为436
mol-1,键能可作为衡量化学键牢固程度的键参数
键长形成共价键的两个原子之间的核间的平衡距离
键能与键长的关系:一般来说,键长越短,键能越大,分子越稳定
键角分子中两个相邻共价键之间的夹角称键角
键角决定分子的立体结构和分子的极性
三、等电子原理1
原子总数相同、价电子总数相同的分子具有相似化学键特征,许多性质是相似的
此原理称为等电子原理2
等电子体的判断和利用判断方法:原子总数相同,价电子总数相同的分子为等电子体运用:利用等电子体的性质相似,空间构型相同,可运用来预测分子空间的构型和性质四、价层电子对互斥模型(VSEPR)基本要点ABn型分子(离子)中中心原子A周围的价电子对的几何构型,主要取决于价电子对数(n),价电子对尽量远离,使它们之间斥力最小
平面三角形1200正四面体109
50MMM直线1800价电子对空间构型432n直线型平面三角型四面体BeCl2,HgCl2BF3,BCl3(CH4,CCl4,NH4+)中心原子价电子都用于形成共价键,不含孤对电子三角锥V型H2O,H2S(NH3;H3O+)中心原子有孤对电子CH4:(sp3杂化)激发杂化3sp3spp2s2s2p2s2C:2p五、杂化轨道理论SP3杂化SP2杂化SP杂化2
杂化轨道的应用范围:杂化轨道只应用于形成σ键或者用来容纳未参加成键的孤对电子
判断下列分子或离子中,中心原子的杂化轨道类型NH4+、NH3、H2O、CH2O、SO2BeCl2、CO2一般方法:1、看中心原子有没有