卜人入州八九几市潮王学校第四单元物质构成的奥秘1、原子的构成其中:核电荷数=质子数=核外电子数=原子序数2、相对原子质量:〔符号为Ar〕〔1〕定义:以一种碳原子〔碳12〕质量的1/12为HY,其他原子的质量跟它相比较所得到的比,作为这种原子的相对原子质量
相对原子质量是一个比值,单位为“1〞一般不写
〔2〕表达式:某原子的实际质量(kg)相对原子质量〔Ar〕=HY碳原子的质量〔kg〕×1/12〔3〕相对原子质量=质子数+中子数3、相对分子质量:〔符号为Mr〕①相对分子质量的定义:化学式中各原子的相对原子质量的总和叫相对分子质量
它与相对原子质量采用的是同一个HY,它是一个比值,单位为“1〞,符号为Mr,一般不写
②计算相对分子质量:相对分子质量=各原子相对原子质量的总和
4、元素:〔1〕元素的概念:具有一样核电荷数〔即核内质子数〕的一类原子的总称为元素
〔2〕元素与原子的区别和联络名称元素只表示一类原子的总称〔质子数一样〕只表示种类,不管个数,是宏观概念原子原子是微观概念,既表示种类,又表示数量含义化学变化中,原子种类数量不变,但最外层电子数可能发生变化区别化学变化中,元素的种类不变,但形态可能发生变化联络元素是同一类原子的总称,原子是构成元素的根本单元〔3〕元素符号:元素用元素符号表示,元素符号是用元素拉丁名称的第一个字母表示的,假设第一个字母一样,那么再附加一个小写字母加以区别
〔4〕元素符号的意义:①元素符号不仅表示一种元素,还表示这种元素的1个原子;②假设元素符号前面加上系数,就只表示该原子的个数,只具有微观意义
③对于用元素符号表示的化学式,它的含义还包括物质及物质的组成
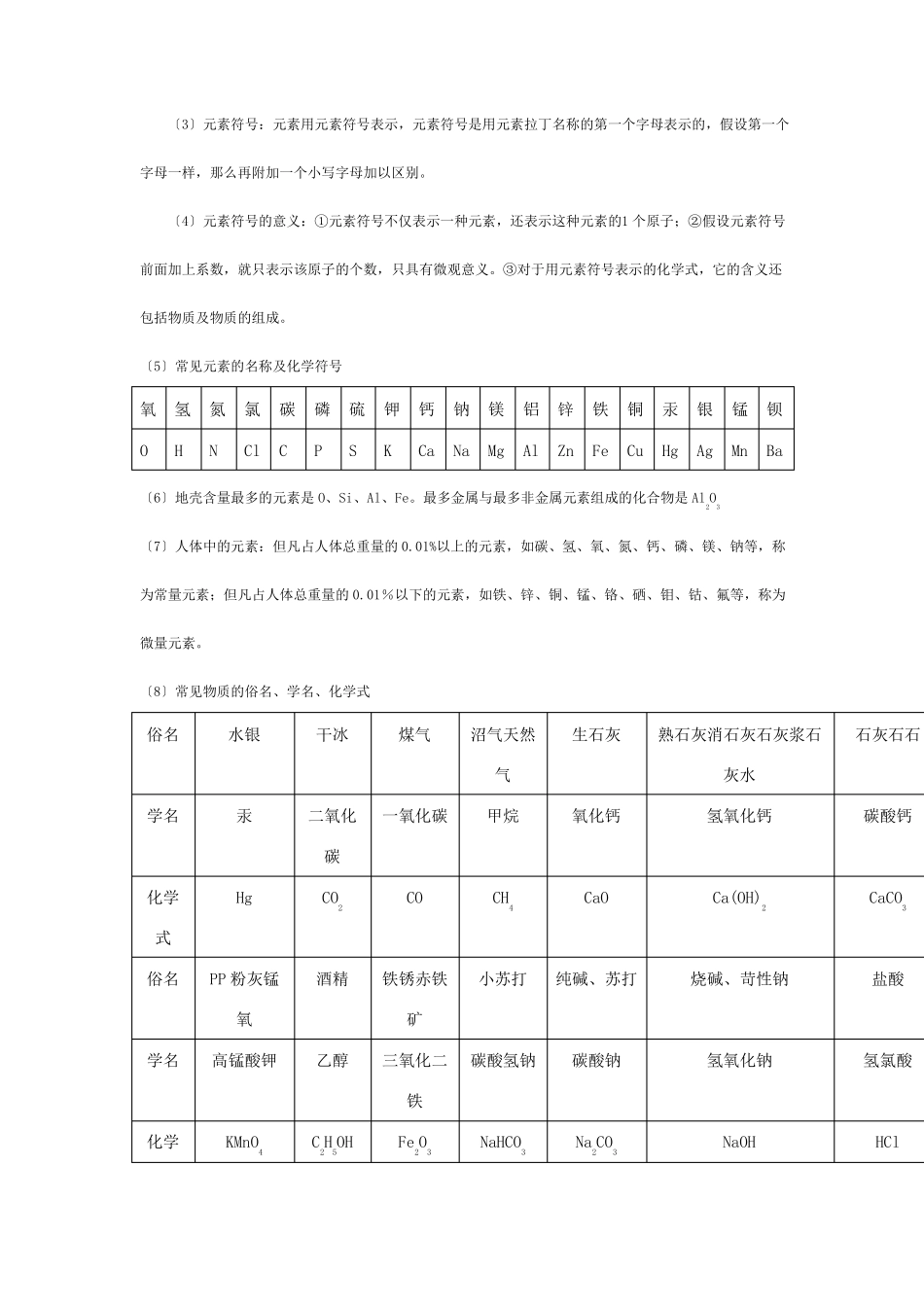
〔5〕常见元素的名称及化学符号氧氢氮氯碳磷硫钾钙钠镁铝锌铁铜汞银锰钡OHNClCPSKCaNaMgAlZnFeCuHgAgMnBa〔6〕地壳含量最多的元素是O、Si、Al、Fe
最多金属与最多非