专题二非金属元素及其化合物课时7氯气的性质及其制备1(2014·江苏高考)在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是()A
氯水的颜色呈浅绿色,说明氯水中含有Cl2B
向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-C
向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+D
向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO【答案】D【解析】氯气是黄绿色气体,氯水中含有氯气而显浅绿色,A正确;Cl-的检验方法:向溶液中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明溶液中含有Cl-,B正确;H++HC-3OCO2↑+H2O,C正确;溶液颜色变成棕黄色,说明生成了氯化铁,有可能是氯水中的HClO将Fe2+氧化成Fe3+,也有可能是氯水中的Cl2将Fe2+氧化成Fe3+,所以不能说明氯水中含有HClO,D错误
2将Cl2分别通入下列四种溶液中,有关现象及结论的说法正确的是()A
试管①中有白色沉淀生成,说明Cl2与水反应生成了盐酸B
试管②中溶液褪色,只是氯气与水反应生成HClO的缘故C
试管③中能产生白色沉淀,说明Cl2具有还原性D
试管④中溶液变红色,说明Cl2具有氧化性【答案】AD【解析】生成白色沉淀AgCl,Ag++Cl-AgCl↓,说明生成了盐酸,A正确;溶液褪色主要是由于Cl2与NaOH反应使碱性消失,B错误;Cl2+SO2+2H2O4H++2Cl-+S2-4O,Ba2++S2-4OBaSO4↓,Cl2被还原成Cl-,说明Cl2有氧化性,C错误;2Fe2++Cl22Fe3++2Cl-,氯气将Fe2+氧化为Fe3+,D正确
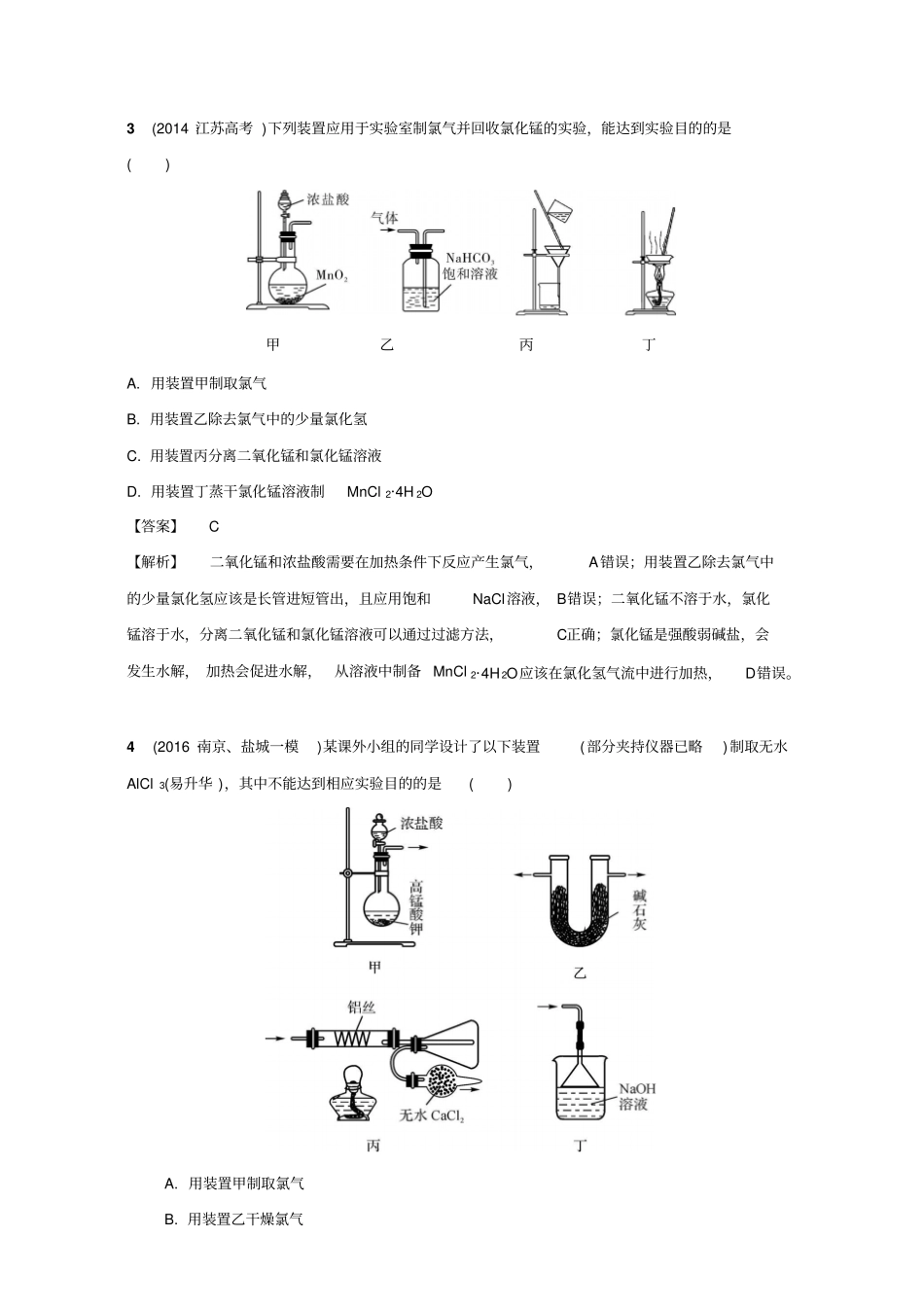
3(2014·江苏高考)下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是()甲乙丙丁A
用装置甲制取氯气B
用装置乙除去氯气中的少量氯化氢C
用装置丙分离