第三节氧化还原反应(1)C+O2==CO2(2)2H2O2==2H2O+O2↑(3)H2+CuO==Cu+H2O(4)2NaOH+H2SO4==Na2SO4+2H2O点燃MnO2△思考:指出下列反应各属于何种类型
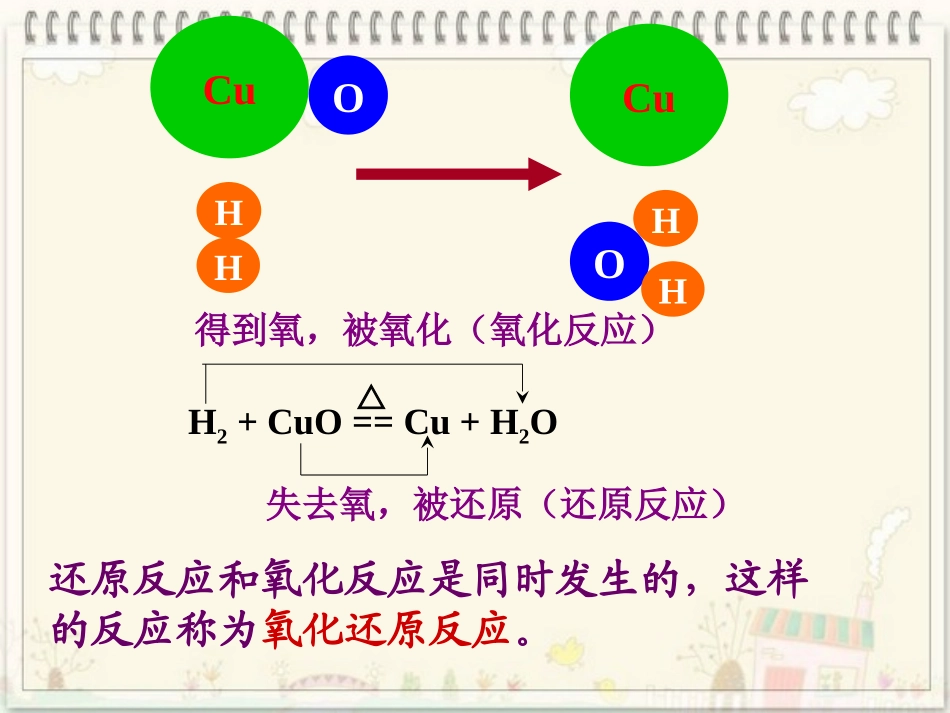
化合反应、氧化反应分解反应置换反应、还原反应复分解反应失去氧,被还原(还原反应)得到氧,被氧化(氧化反应)CuOHHHHCuOH2+CuO==Cu+H2O△还原反应和氧化反应是同时发生的,这样的反应称为氧化还原反应
一、氧化还原反应思考:分析下列氧化还原反应中各种元素的化合价在反应前后有无变化
2CuO+C==2Cu+CO2↑H2O+C==H2+COCuO+H2==Cu+H2O+200+4+100+2+200+1高温高温△在氧化还原反应中,某些元素的化合价在反应前后发生了变化
一、氧化还原反应1
氧化还原反应特征:元素化合价发生了变化(判断依据)氧化剂失氧,被还原(还原反应)得氧,被氧化(氧化反应)H2+CuO==Cu+H2O△0+20+1化合价升高,被氧化化合价降低,被还原思考:氧化还原反应中,为什么元素化合价在反应前后发生改变呢
还原剂还原产物氧化产物从微观的角度(原子结构)分析下面的这两个从微观的角度(原子结构)分析下面的这两个反应化合价升降的原因:反应化合价升降的原因:2NaCl2NaCl2Na2Na++ClCl22HH22++ClCl222HCl2HCl00+1-100+1-12NaCl2NaCl2Na2Na++ClCl22Na:化合价升高,因为失去电子Cl:化合价降低,因为得到电子00+1-1化合价升降:电子的得失HH22++ClCl222HCl2HCl00+1-1H:化合价升高,因为共用电子对偏离Cl:化合价降低,因为共用电子对偏向化合价升降:电子对的偏移一、氧化还原反应2
氧化还原反应实质:电子转移(得失或偏移)1
氧化还原反应特征:元素化合价发生