药品文献评价指导原则国家食品药品监督管理局药品评价中心一、前言开展药品上市后研究对于准确掌握药品信息,正确评价药品的安全性和有效性,指导临床合理用药具有极其重要意义
文献评价是药品上市后研究的主要方法之一,与试验性研究相比具有很多优点,如耗时相对较短、研究费用相对较低、可以系统评价药品某一方面特征等
目前我国很多药品生产企业不熟悉如何系统开展文献评价,或者开展文献评价不够规范,主要表现为文献资料获取过程中信息收集不全面、分析评价方法不规范、以及结果解释和运用不合理
制定本指导原则旨在规范上市药品文献评价流程,为药品生产企业向药品监督管理部门提交高质量的文献评价报告提供指导;该指导原则也可供其他科研人员或临床医生参考
本指导原则借鉴了循证医学(EBM)证据分类、分级、严格评价和不断更新的理念与方法,参考了卫生技术评估(HTA)综合评价卫生技术有效性、安全性的指标与形式,引进了Cochrane系统评价规范化操作流程和全程质量控制的方法
本指导原则为技术指导原则,仅反映药品评价中心当前对上市药品文献评价的观点
本指导原则不涉及管理层面的问题,如上市药品文献评价的管理、文献评价机构与人员的资质等
为使读者更好地理解本指导原则,现对本指导原则中的主要术语定义如下:1
“文献”包括已公开发表的文献、未公开发表的文献(即灰色文献)等
“文献评价”是指尽可能全面系统地收集一定时间范围内、特定药品的安全性、有效性研究文献,在对文献进行质量评价、资料提取、归纳整理的基础上,进行综合地分析评价,并形成评价报告的过程
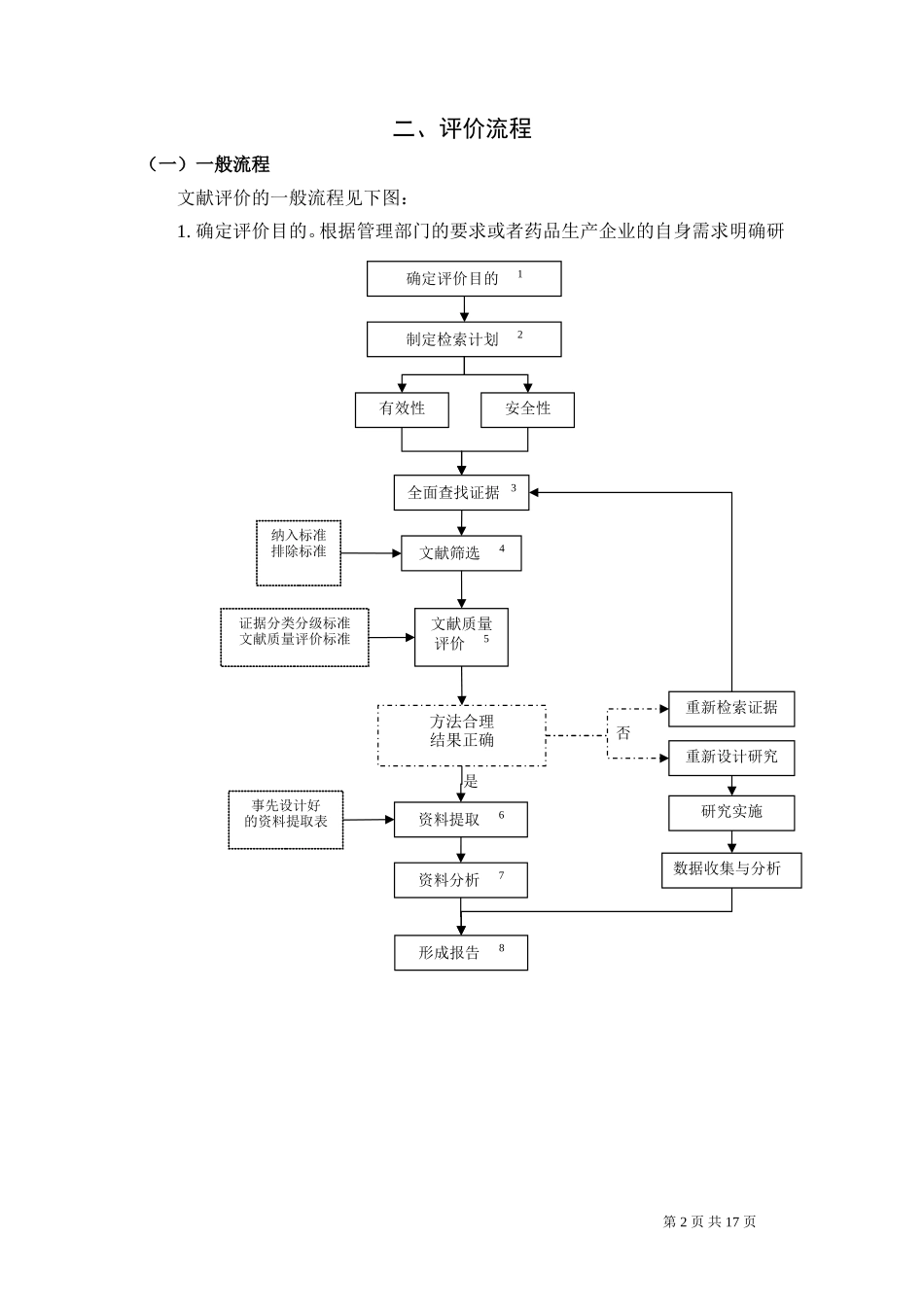
第1页共17页二、评价流程(一)一般流程文献评价的一般流程见下图:1
确定评价目的
根据管理部门的要求或者药品生产企业的自身需求明确研第2页共17页确定评价目的1制定检索计划2有效性安全性全面查找证据3纳入标准排除标准证据分类分级标准文献质量评价标准文献筛选4文献质量评价5资料提