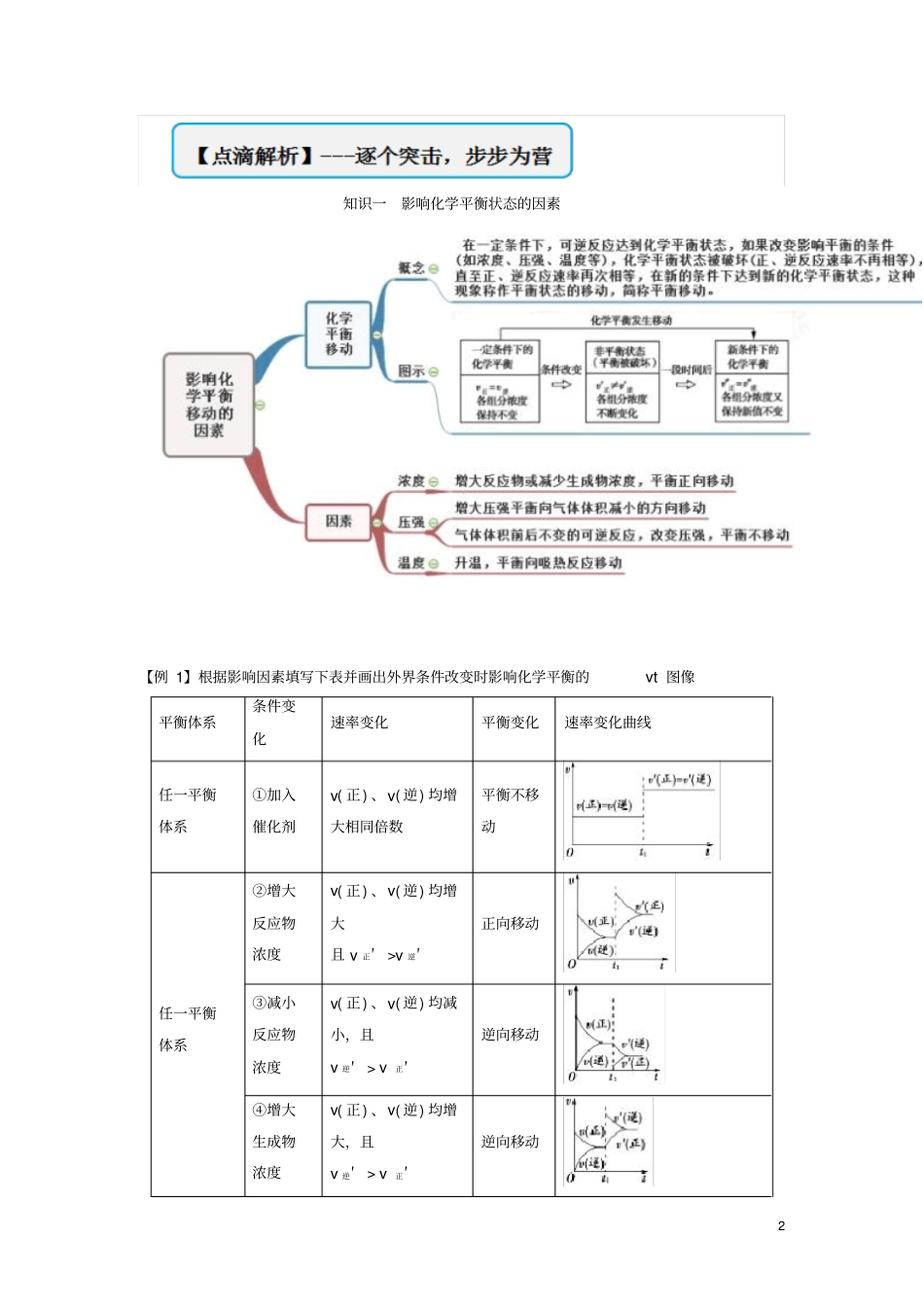
1专题07化学平衡(二)2知识一影响化学平衡状态的因素【例1】根据影响因素填写下表并画出外界条件改变时影响化学平衡的vt图像平衡体系条件变化速率变化平衡变化速率变化曲线任一平衡体系①加入催化剂v(正)、v(逆)均增大相同倍数平衡不移动任一平衡体系②增大反应物浓度v(正)、v(逆)均增大且v正′>v逆′正向移动③减小反应物浓度v(正)、v(逆)均减小,且v逆′>v正′逆向移动④增大生成物浓度v(正)、v(逆)均增大,且v逆′>v正′逆向移动3⑤减小生成物浓度v(正)、v(逆)均减小,且且v正′>v逆′正向移动当正反应为放热反应时升高温度v(正)、v(逆)均增大,且v逆′>v正′逆向移动降低温度v(正)、v(逆)均减小,且且v正′>v逆′正向移动当正反应为吸热反应时降低温度v(正)、v(逆)均减小,且v逆′>v正′逆向移动升高温度v(正)、v(逆)均增大,且且v正′>v逆′正向移动以aA(g)+bB(g)cC(g)为例当时⑥增大压强或升高温度v(正)、v(逆)均增大,且v逆′>v正′逆向移动⑦减小压强或降低温度v(正)、v(逆)均减小,且且v正′>v逆′正向移动4当时增大压强v(正)、v(逆)均增大,且且v正′>v逆′正向移动减少压强v(正)、v(逆)均减小,且v逆′>v正′逆向移动当时增大压强v(正)、v(逆)同时增大,且且v正′=v逆′平衡不移动降低压强v(正)、v(逆)同时减小,且且v正′=v逆′平衡不移动【变式】1
往FeCl3溶液中滴加少量KSCN溶液,溶液呈红色,发生如下反应:FeCl3+3KSCN3KCl+Fe(SCN)3(棕黄色)(无色)(无色)(红色)下列说法中正确的是()A
往上述溶液中滴入Fe2(SO4)3溶液,溶液红色变浅B
往上述溶液中滴入NH4SCN溶液,溶液红色不变C
往上述溶液中加入铁粉,溶液红色加深D
往上述溶液中滴入NaOH溶液,溶液红色变浅