第4节难溶电解质的溶解平衡考试说明1.了解难溶电解质的沉淀溶解平衡
2.了解难溶电解质的沉淀转化的本质
3.了解溶度积的含义及其表达式,能进行相关的计算
命题规律本节内容是历届各地高考的热点,考查点有三个:一是考查溶解平衡的移动及平衡的建立;二是结合图像,考查溶度积的应用及影响因素;三是沉淀反应在生产、科研和环保中的应用
考点1沉淀溶解平衡及其应用1.沉淀溶解平衡(1)概念在一定温度下,当难溶电解质溶于水形成饱和溶液时,沉淀溶解速率和沉淀生成速率相等的状态
(2)溶解平衡的建立(3)特点(4)表示AgCl在水溶液中的电离方程式为AgCl===Ag++Cl-
AgCl的溶解平衡方程式为AgCl(s)Ag+(aq)+Cl-(aq)
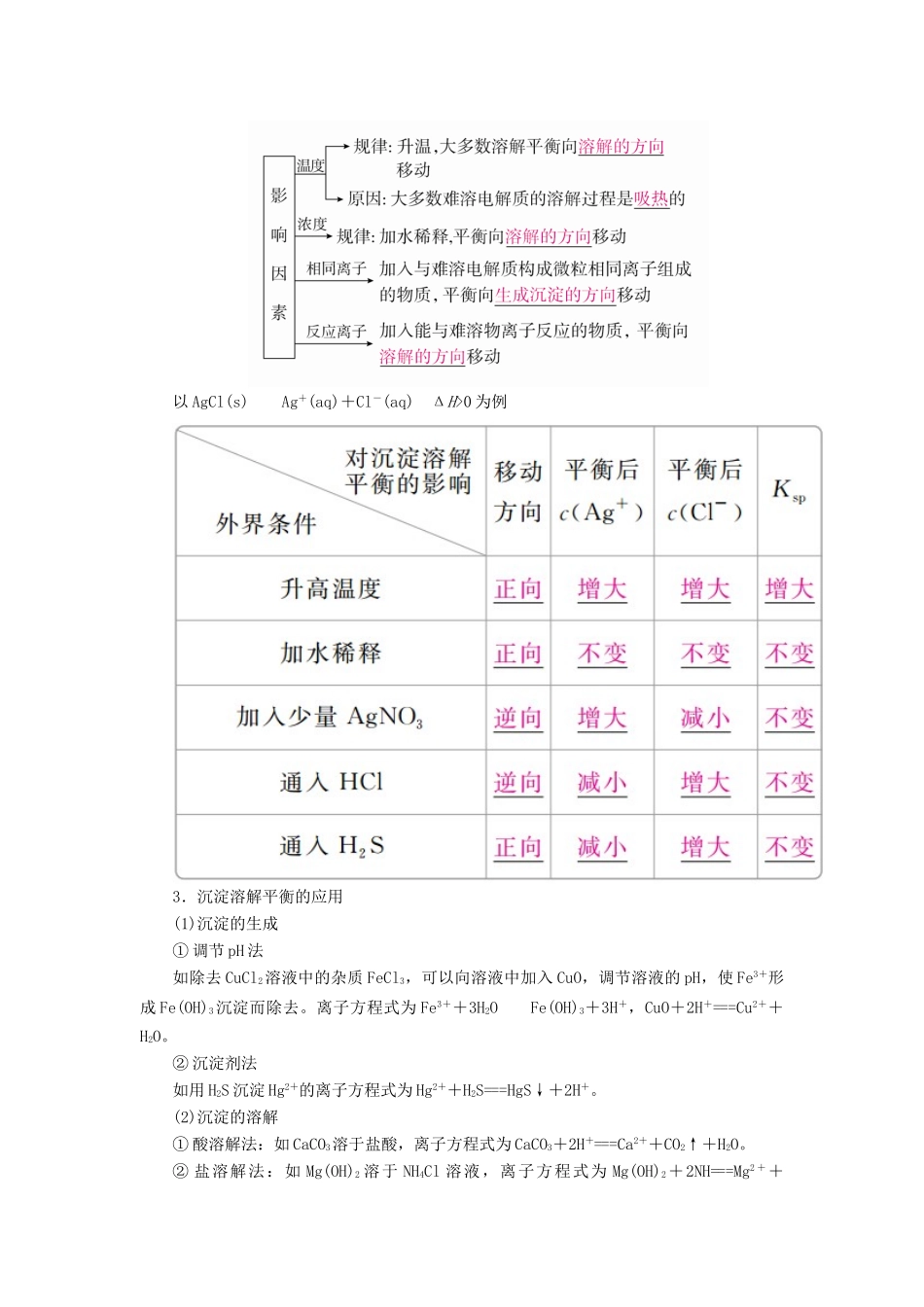
2.影响沉淀溶解平衡的因素以AgCl(s)Ag+(aq)+Cl-(aq)ΔH>0为例3.沉淀溶解平衡的应用(1)沉淀的生成①调节pH法如除去CuCl2溶液中的杂质FeCl3,可以向溶液中加入CuO,调节溶液的pH,使Fe3+形成Fe(OH)3沉淀而除去
离子方程式为Fe3++3H2OFe(OH)3+3H+,CuO+2H+===Cu2++H2O
②沉淀剂法如用H2S沉淀Hg2+的离子方程式为Hg2++H2S===HgS↓+2H+
(2)沉淀的溶解①酸溶解法:如CaCO3溶于盐酸,离子方程式为CaCO3+2H+===Ca2++CO2↑+H2O
②盐溶解法:如Mg(OH)2溶于NH4Cl溶液,离子方程式为Mg(OH)2+2NH===Mg2++2NH3·H2O
③配位溶解法:如Cu(OH)2溶于NH3·H2O溶液,离子方程式为Cu(OH)2+4NH3·H2O===[Cu(NH3)4]2++2OH-+4H2O
(3)沉淀的转化①实质:沉淀溶解平衡的移动
②特征a.一般说来,溶解度小的沉淀转化为溶解度更小的沉淀容易实现
如:AgNO3――→AgCl―