第3节盐类的水解考试说明1.了解盐类水解的原理
2.了解影响盐类水解程度的主要因素
3.了解盐类水解的应用
命题规律本节内容是高考考查的重点与热点,主要考点有四个:一是水解方程式的书写;二是水解平衡的影响因素及水解平衡移动;三是溶液中离子浓度大小的比较和守恒关系;四是盐类水解在工农业生产和实验中的应用
考点1盐类的水解及其规律1.定义在溶液中盐电离出来的离子跟水电离产生的H+或OH-结合生成弱电解质的反应
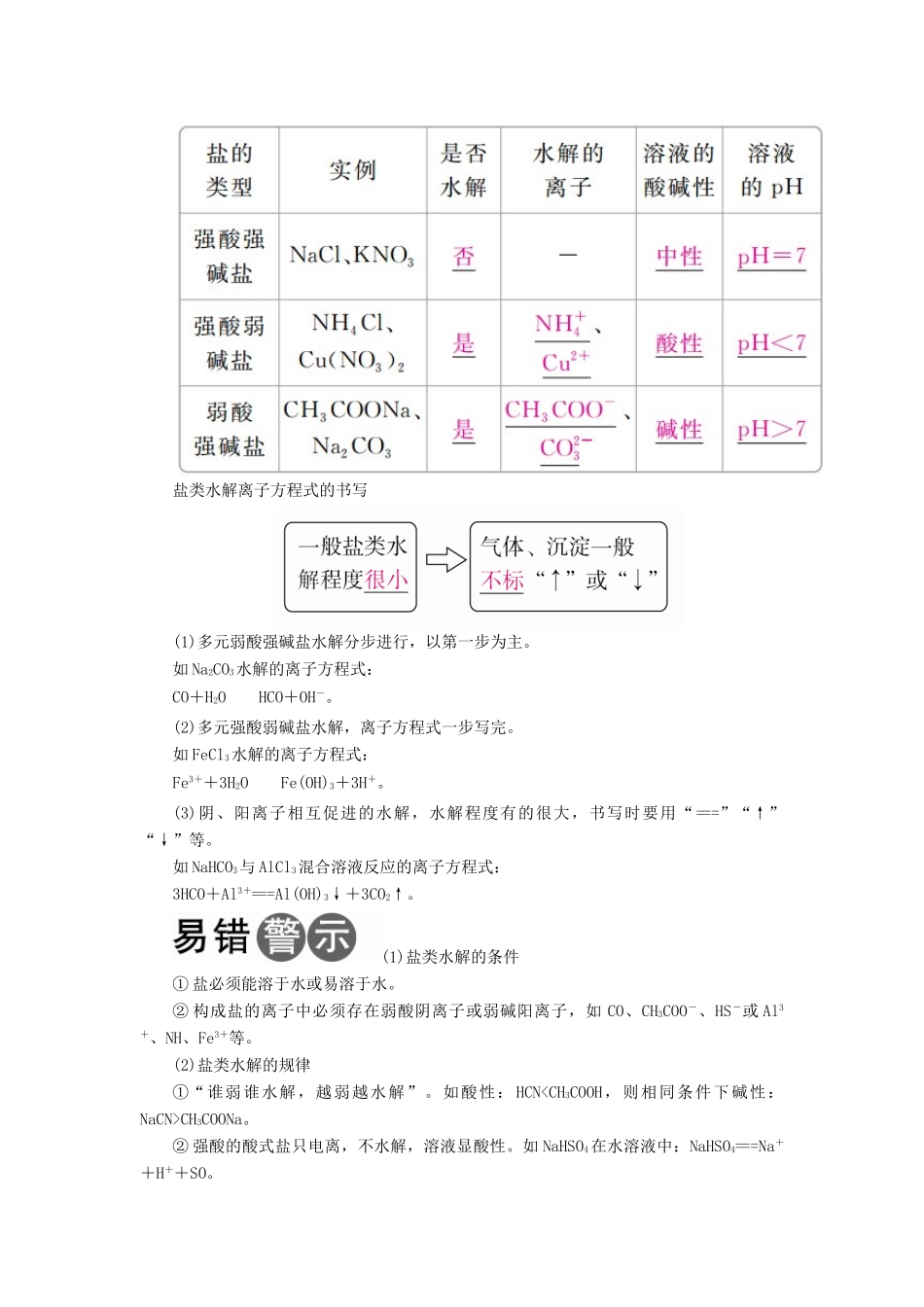
2.实质3.特点4.规律有弱才水解,越弱越水解,谁强显谁性,同强显中性
盐类水解离子方程式的书写(1)多元弱酸强碱盐水解分步进行,以第一步为主
如Na2CO3水解的离子方程式:CO+H2OHCO+OH-
(2)多元强酸弱碱盐水解,离子方程式一步写完
如FeCl3水解的离子方程式:Fe3++3H2OFe(OH)3+3H+
(3)阴、阳离子相互促进的水解,水解程度有的很大,书写时要用“===”“↑”“↓”等
如NaHCO3与AlCl3混合溶液反应的离子方程式:3HCO+Al3+===Al(OH)3↓+3CO2↑
(1)盐类水解的条件①盐必须能溶于水或易溶于水
②构成盐的离子中必须存在弱酸阴离子或弱碱阳离子,如CO、CH3COO-、HS-或Al3+、NH、Fe3+等
(2)盐类水解的规律①“谁弱谁水解,越弱越水解”
如酸性:HCNCH3COONa
②强酸的酸式盐只电离,不水解,溶液显酸性
如NaHSO4在水溶液中:NaHSO4===Na++H++SO
③弱酸的酸式盐,在溶液中既电离又水解,溶液的酸碱性取决于酸式酸根离子的电离程度和水解程度的相对大小
a.若电离程度小于水解程度,溶液呈碱性
如NaHCO3溶液中:HCOH++CO(次要),HCO+H2OH2CO3+OH-(主要)
b.若电离程度大于水解程度,溶液显酸性
如NaHSO3溶液中:HSOH++SO(主