课时2铁、铜的获取及应用[考纲导航]知识条目必考要求加试要求选考分布2015201620179月10月4月10月4月(1)自然界铁、铜的存在形式,铁、铜的物理性质aa(2)工业炼铁的反应原理bb27(3)铁、铜的化学性质(跟某些非金属、酸、盐的反应)bb1427272727(4)Fe2+、Fe3+的性质及转化cc32(3)32(4)32(3)24(5)检验Fe2+、Fe3+的常用方法bc28(6)不锈钢的主要组成元素及其用途a考点一铁的性质、铁的氧化物与氢氧化物[主干精讲]1.铁的存在和物理性质(1)铁的存在铁在自然界中主要以化合态的形式存在,陨铁以游离态的形式存在
常见的铁矿:磁铁矿[主要成分为Fe3O4(填化学式,下同)],赤铁矿(主要成分为Fe2O3),黄铁矿(主要成分为FeS2)
(2)铁的物理性质铁是电和热的良导体,能被磁铁吸收,纯铁具有很强的抗腐蚀能力
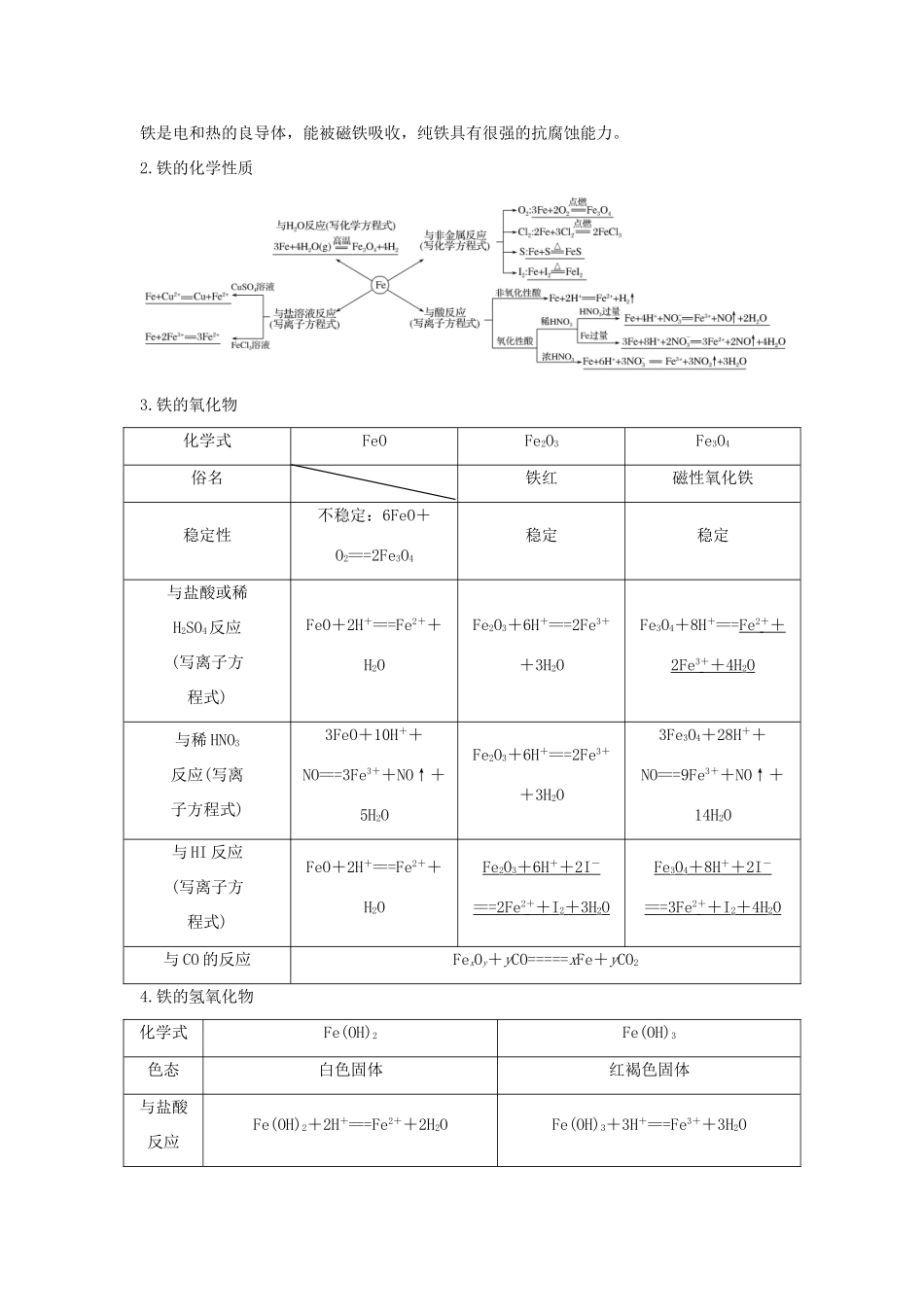
铁的化学性质3
铁的氧化物化学式FeOFe2O3Fe3O4俗名铁红磁性氧化铁稳定性不稳定:6FeO+O2===2Fe3O4稳定稳定与盐酸或稀H2SO4反应(写离子方程式)FeO+2H+===Fe2++H2OFe2O3+6H+===2Fe3++3H2OFe3O4+8H+===Fe2++2Fe3++4H2O与稀HNO3反应(写离子方程式)3FeO+10H++NO===3Fe3++NO↑+5H2OFe2O3+6H+===2Fe3++3H2O3Fe3O4+28H++NO===9Fe3++NO↑+14H2O与HI反应(写离子方程式)FeO+2H+===Fe2++H2OFe2O3+6H++2I-===2Fe2++I2+3H2OFe3O4+8H++2I-===3Fe2++I2+4H2O与CO的反应FexOy+yCO=====xFe+yCO24
铁的氢氧化物化学式Fe(OH)2Fe(OH)3色态白色固体红褐色固体与盐酸反应F