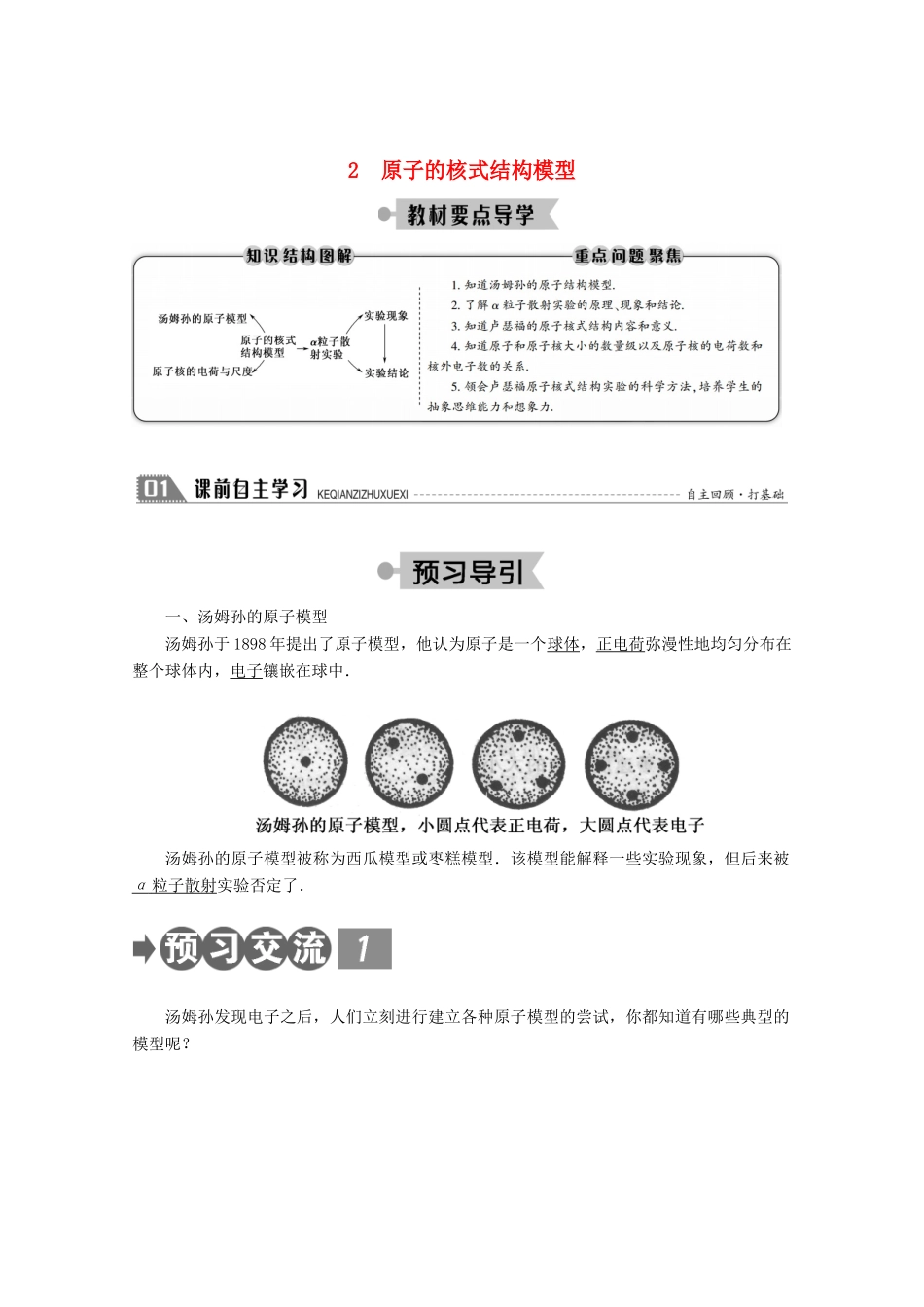
2原子的核式结构模型一、汤姆孙的原子模型汤姆孙于1898年提出了原子模型,他认为原子是一个球体,正电荷弥漫性地均匀分布在整个球体内,电子镶嵌在球中.汤姆孙的原子模型被称为西瓜模型或枣糕模型.该模型能解释一些实验现象,但后来被α粒子散射实验否定了.汤姆孙发现电子之后,人们立刻进行建立各种原子模型的尝试,你都知道有哪些典型的模型呢
提示:(1)勒纳德的动力子模型:原子内部的电子与相应的正电荷组成一个中性的“刚性配偶体”,他取名为动力子,无数动力子漂浮于原子太空内.(2)长冈半太郎的土星型模型:1904年,他根据麦克斯韦的土星环理论推测原子的结构,提出了一个土星模型,它实际上已经包含了核模型的基本思想,只是对核的大小的数量级及稳定性等问题没有给出足够的重视.(3)汤姆孙的“枣糕模型”.(4)卢瑟福的核式结构模型.(5)玻尔模型.后面的三种模型教材中已经做了阐述.二、α粒子散射实验1.从放射性物质中发射出来的快速运动的粒子,实质是失去两个电子的氦原子核,带两个单位正电荷,质量为氢原子质量的4倍.2.实验结果绝大多数α粒子穿过金箔后,基本沿原方向前进.少数α粒子发生大角度偏转,偏转角甚至大于90°
3.卢瑟福的核式结构模型1911年由卢瑟福提出,在原子中心有一个很小的核,叫原子核.它集中了全部的正电荷和几乎全部的质量,电子在核外空间运动.在α粒子散射实验中,偏转角大的α粒子与偏转角小的α粒子相比,谁离原子核更近一些
提示:α粒子与原子核之间有相互作用的库仑斥力,偏转角大,意味着库仑力大,因而也就越靠近原子核.三、原子核的电荷与尺度1.原子内的电荷关系各种元素的原子核的电荷数与含有的电子数相等,非常接近于它们的原子序数.2.原子核的组成原子核是由质子和中子组成的,原子核的电荷数就等于原子核中的质子数.3.原子核的大小实验确定的原子核半径R的数量级为10-15_m,而原子的半径的数量级是