第一章物质结构元素周期律谷城一中高一化学组2012
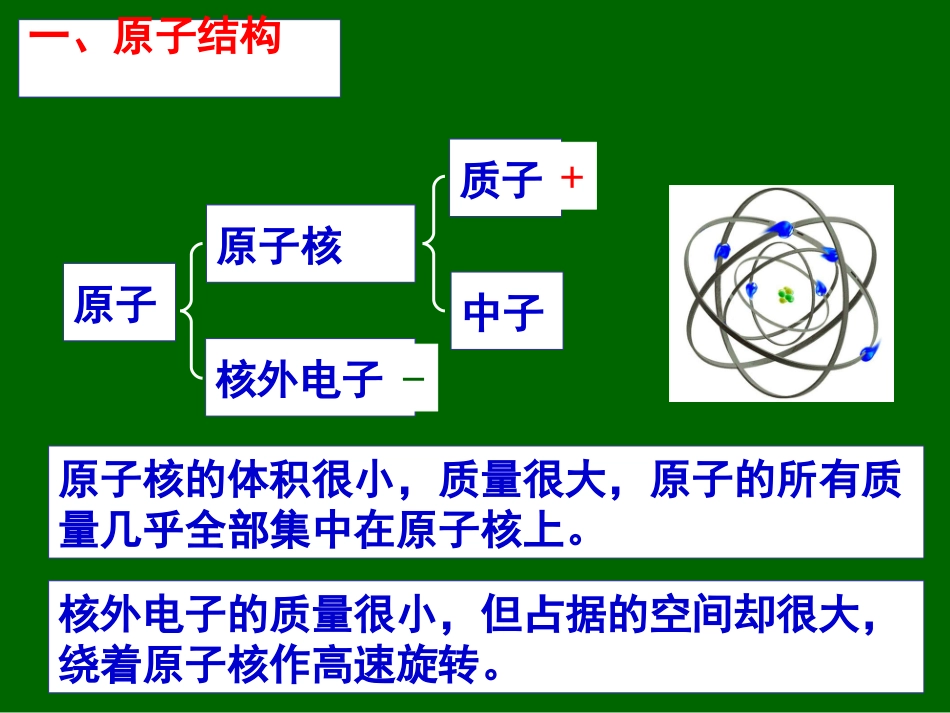
2一、原子结构原子原子核核外电子质子中子+-原子核的体积很小,质量很大,原子的所有质量几乎全部集中在原子核上
核外电子的质量很小,但占据的空间却很大,绕着原子核作高速旋转
1、一组数量关系原子序数=质子数=核电荷数=核外电子数质量数(A)=质子数(Z)+中子数(N)原子的符号:XZA例1:在中有个质子,个中子,个电子,其质量数为
Cl1735171817352、元素、同位素、核素元素:具有相同核电荷数(质子数)的同类原子的总称
同位素:质子数相同而中子数不同的同种元素原子之间互称为同位素
H11H12H13H氕D氘T氚O816O817O818C612C613C614同位素之间的物理性质相差较大,但化学性质几乎完全相同
核素:具有一定数目质子和一定数目中子的一种原子叫做一种核数
元素的种类是由质子数决定的
核素(原子)的种类是由质子数和中子数共同决定的
现在我们发现了120多种元素,但我们却发现了1000多种核素(原子)
U92235H133、核素的相对原子质量核素的相对原子质量=一个核素原子的实际质量一个12C原子的实际质量×112元素的相对原子质量该元素各种核素的相对原子质量和其所占的原子个数百分比计算出来的平均值
元素的近似相对原子质量该元素各种核素的质量数和其所占的原子个数百分比计算出来的平均值
M=A1×n1%+A2×n2%+A3×n3%+……4、原子核外电子的排布规律①按照能量由低到高,分层排布
②每层上最多能够容纳的电子数为2n2
+KLMNOPQ低高③电子总是先占据能量较低的电子层,然后再占据能量较高的电子层
且最外层不超过8个电子,次外层不超过18个电子,倒数第三层不超过32个电子
281832练习:写出前18号元素的元素名称、元素符号、并画出原子结构示意图(简图)
+11氢H+22氦He1+32锂Li18