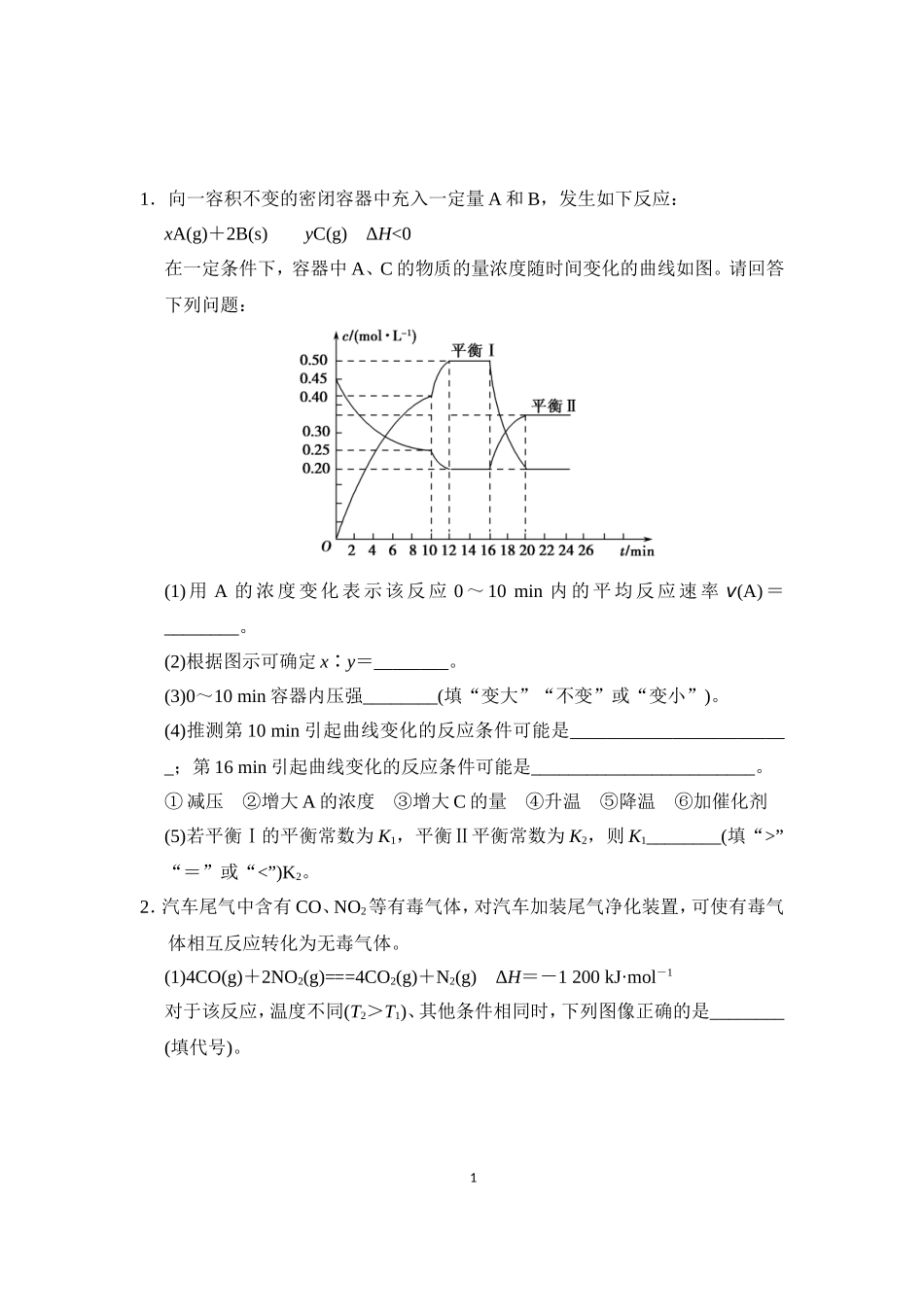
1.向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s)yC(g)ΔH”“=”或“0某小组通过实验研究该反应(反应过程中体积变化忽略不计)
反应体系中各组分的起始量如下表:组分HCOORH2OHCOOHROH物质的量浓度1
522/mol·L-1甲酸酯转化率在温度T1下随反应时间(t)的变化如图:根据上述条件,计算不同时间范围内甲酸酯的平均反应速率,结果见下表:反应时间/min0~510~1520~2530~3540~4550~5575~80平均速率/(10-3mol·L-1·min-1)1
0(1)该反应的平衡常数K的表达式为________(不要求计算);T1温度下平衡体系中c(ROH)为________mol·L-1
(2)15~20min范围内用甲酸酯表示的平均反应速率为____________mol·L-1·min-1(不要求写出计算过程)
(3)根据题给数据分析,从影响反应速率的角度来看,生成物甲酸在该反应中还起到了________的作用
4.铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质
(1)在一定温度下,氧化铁可以与一氧化碳发生反应:Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g)
已知该反应在不同温度下的平衡常数如下表:温度/℃100011501300平衡常数64
9请回答下列问题:①该反应的平衡常数表达式K=________,ΔH________0(填“>”、“<”或“=”)
②在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各31
0mol,反应经过10min后达到平衡
求该时间范围内反应的平均反应速率v(CO2)=________,CO的平衡转化率为________
③欲提高②中CO的平衡转