复习回顾:酸(H++酸根离子)1
酸加入紫色石蕊试液,溶液变色,加入无色酚酞,溶液,这说明了酸中含有
盐酸(HCl)、硫酸(H2SO4)等碱(金属离子+OH-)1
常见的碱有2
在碱中加入紫色石蕊试液变色,加入无色酚酞溶液变色,这说明了碱中含有
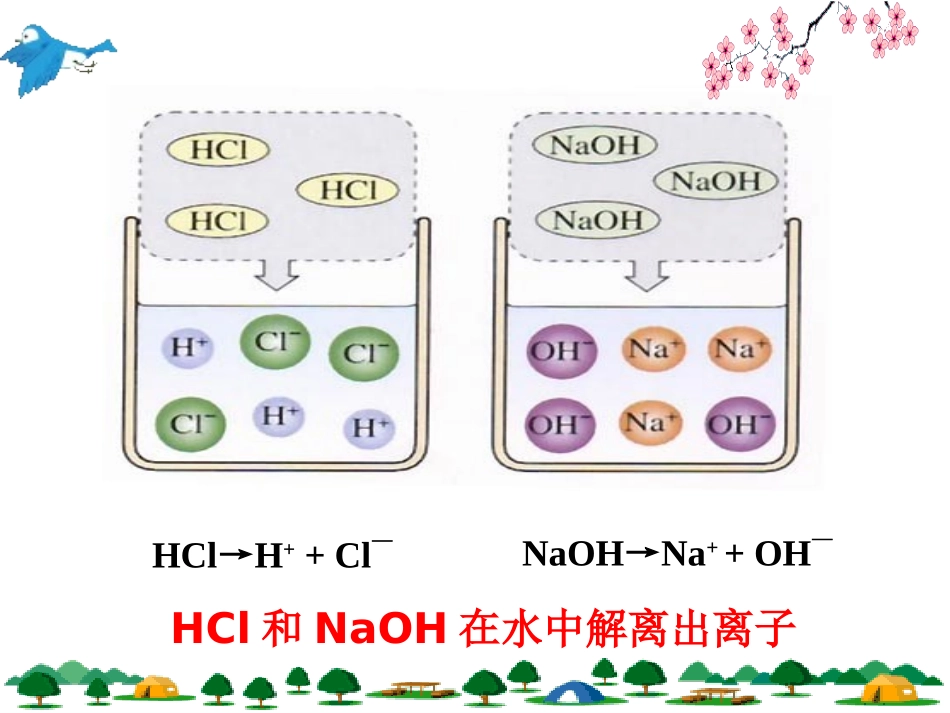
氢氧化钠(NaOH)氢氧化钙(Ca(OH)2)等蓝红OH-红不变色H+HCl→H++Cl—NaOH→Na++OH—HCl和NaOH在水中解离出离子1、提出问题:酸和碱之间会发生什么反应2、猜想与假设:酸和碱之间能发生应,并有水生成3、设计实验方案4、进行实验探究5、分析结果,得出结论演示实验:在NaOH溶液中滴加盐酸,振荡,观察现象
•对这个实验的现象的判断,可能存在两种观点:1、盐酸和氢氧化钠溶液没有发生反应;2、二者反应了,但是没有明显现象
设计实验方案滴加酚酞溶液方案一:NaOH溶液溶液滴加盐酸溶液(无色)(红色)(红色恰好褪为无色)方案二:盐酸滴加酚酞溶液溶液溶液滴加NaOH溶液(无色)振荡振荡(无色)(无色)在氢氧化钠溶液中加入盐酸化学方程式:NaOH+HCl=NaCl+H2O微观展示酸和碱之间会发生什么反应
实验现象:得出结论:为什么要加入酚酞指示剂
借以判断反应有无发生什么时候酸和碱恰好完全反应
溶液恰好由红色变为无色溶液由红色变为无色酸和碱能反应反应后生成了什么物质
现在烧杯内溶液中溶质是什么呢
氯化钠和水氯化钠盐酸与氢氧化钠反应的本质:H++OH-=H2O酸溶液中的氢离子和碱溶液中的氢氧根离子反应生成水的过程
在水溶液中能解离出金属离子和酸根离子是什么物质
(水在常温下很稳定,不会分解)HCl+NaOH===NaCl+H2O碱酸金属离子酸根离子Cl_SO4_CO3_NO3_等盐中和反应:盐:由金属离子和酸根离子构成的化合物
中和反应不是基本反应类型酸和碱作用生成盐和水的反应
Na+、Ca2+、M