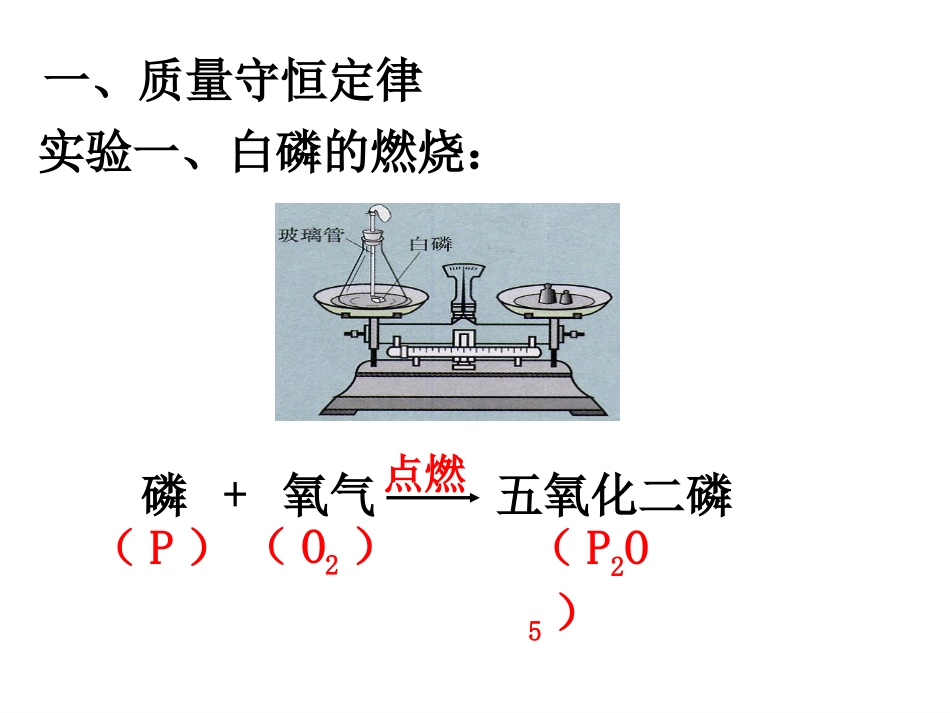
课题1质量守恒定律一、质量守恒定律实验一、白磷的燃烧:磷+氧气五氧化二磷点燃(P)(O2)(P2O5)实验二、铁与硫酸铜溶液的反应:铁+硫酸铜铜+硫酸亚铁(Fe)(CuSO4)(Cu)(FeSO4)银白色蓝色溶液红色浅绿色溶液参加化学反应的各物质的质量总和等于反参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
应后生成的各物质的质量总和
1、质量守恒定律的内容:注意:1、质量守恒定律适用于一切化学反应;2、质量守恒定律研究的是质量守恒,不是体积守恒;3、守恒的范围是“参加化学反应的各物质”,没有参加反应的物质,不能计算在内
实验三、碳酸钠粉末与盐酸反应:实验四、镁条的燃烧:镁+氧气氧化镁点燃碳酸钠+盐酸氯化钠+二氧化碳+水(Na2CO3)(HCl)(NaCl)(CO2)(H2O)(Mg)(O2)(MgO)思考:1、验证质量守恒定律时,必须用到什么仪器
托盘天平2、验证质量守恒定律时,对实验装置有什么要求
密封五个不变两个改变一个可变——分子的数目可能改变宏观微观原子的种类不变;原子的数目不变;原子的质量不变;宏观:物质的种类一定改变;微观:分子的种类一定改变;2、对质量守恒定律的理解:元素的种类不变;元素的质量不变;3、质量守恒定律的应用:1)利用质量守恒定律进行简单的计算;2、已知化学反应A+B==C+D中,A与B参加反应时的质量比为3:2,若反应后生成C与D共10克,则反应用掉A的质量为克
1、化学反应A+B==C中,3gA和足量B反应,可得11gC
如有12gA,能和_____gB完全反应
2)运用质量守恒定律解释化学反应中的一些简单的现象和问题;(1)氯酸钾受热分解后,剩余固体的质量比原反应物的质量轻
(2)镁条在空气中燃烧后,生成物的质量比原来镁条的质量增加
3)判断化学反应中某种物质的组成;1、已知石蜡是蜡烛的主要成分,蜡烛在空气中完全燃烧后的产物