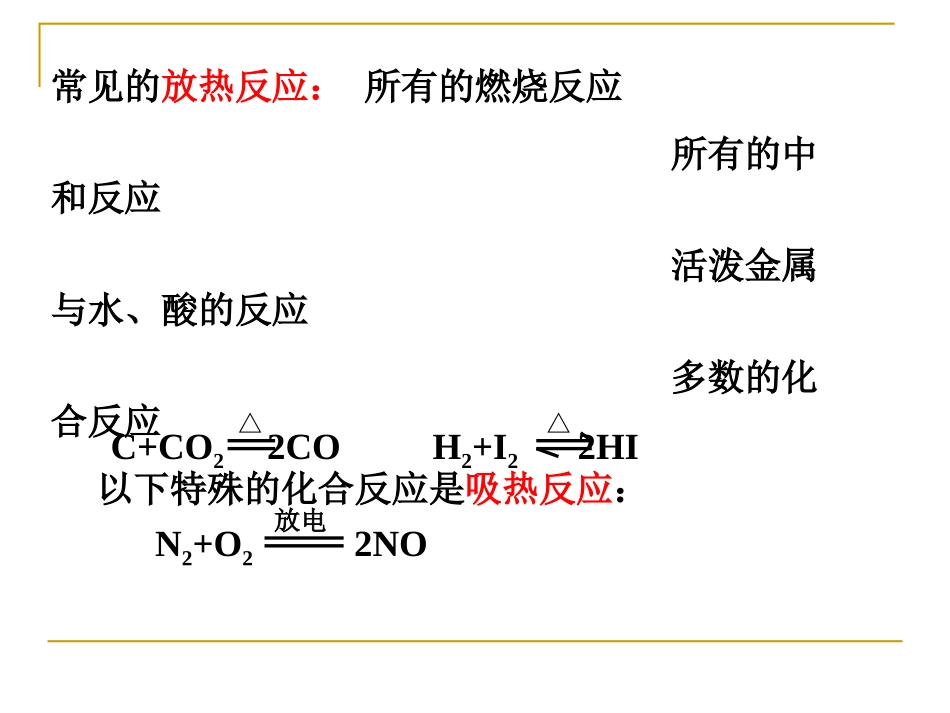
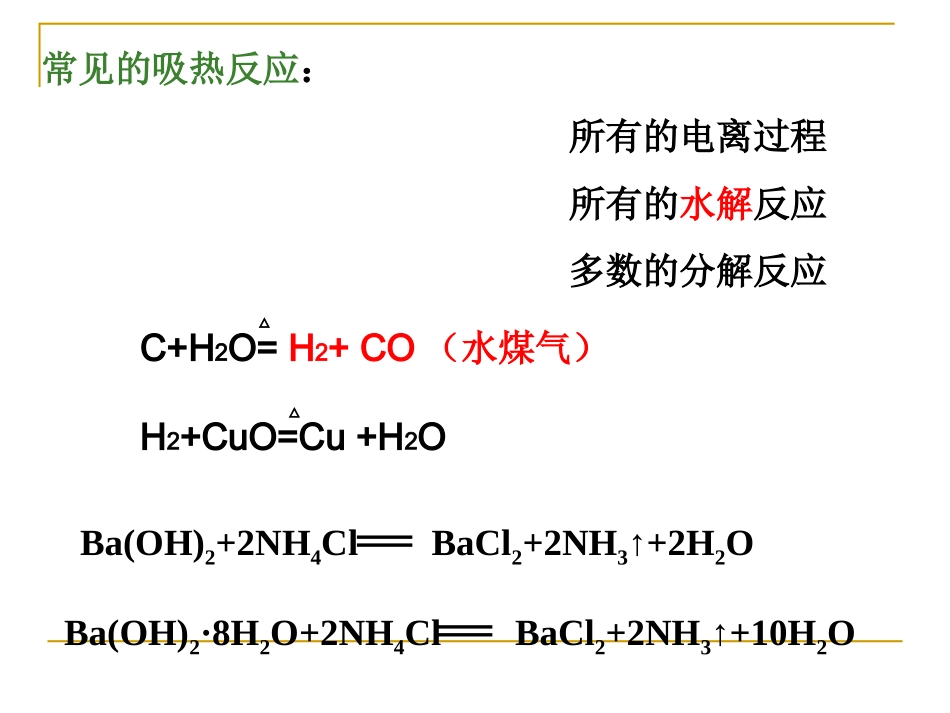
专题1化学反应与能量变化第一单元化学反应中的热效应化学反应的焓变常见的放热反应:所有的燃烧反应所有的中和反应活泼金属与水、酸的反应多数的化合反应以下特殊的化合反应是吸热反应:C+CO22COH2+I22HI△△N2+O22NO放电常见的吸热反应:所有的电离过程所有的水解反应多数的分解反应Ba(OH)2+2NH4ClBaCl2+2NH3↑+2H2OBa(OH)2·8H2O+2NH4ClBaCl2+2NH3↑+10H2OC+H2O=H2+CO(水煤气)H2+CuO=Cu+H2O△△一、反应热焓变1、概念:化学反应过程中所吸收或放出的热量称为化学反应的反应热
在恒温、恒压下,化学反应过程中吸收或放出的热量称为反应的焓变
2、符号:△H单位:kJ/mol3、规定放热:△H0反应物分子断键时吸收的能量☆化学反应过程中为什么会有能量的变化呢
反应物分子断键时吸收的能量放热反应生成物分子成键时释放的能量宏观:能量守恒作用微观:断键,成键作用;反应物的总能量高生成物的总能量低生成物的总能量高反应物的总能量低放热反应吸热反应反应物的总能量=生成物的总能量+放出的热量生成物的总能量=反应物的总能量+吸收的热量化学反应的过程,可以看成是能量的“贮存”或“释放”的过程化学反应中,化学键的断裂和形成是反应过程中有能量变化的本质原因
△H=E反总键能-E生总键能练习:化学反应可视为旧键断裂和新键形成的过程
化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量
已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol1):P—P:198P—O:360O=O:498则反应P4(白磷)+3O2=P4O6的反应热△H为()A.-1638kJ·mol1B.+1638kJ·mol1C.-126kJ·mol1D.+126kJ·mol1A二、热化学方程式:1、概念:能够表示反