第3讲氧化还原反应【2021·备考】最新考纲素养落地1
通过实验事实了解氧化还原反应的本质是电子的转移
了解常见的氧化剂、还原剂和生产生活中常见的氧化还原反应
微观与宏观相结合,多视角、多层次地认识氧化还原反应的特征、实质及规律;运用分析、推理等方法构建氧化还原计算、配平的思维模型,通过实验探究验证并加深对物质氧化性、还原性的理解
『知识梳理』一、氧化还原反应1
氧化还原反应本质和特征2
基本概念及相互关系概括为“升失氧、降得还,剂性一致、其他相反”例如,反应Cu+2H2SO4(浓)=====CuSO4+SO2↑+2H2O中,氧化剂是浓H2SO4,还原剂是Cu,氧化产物是CuSO4
生成1molSO2时转移电子数目为2NA,被还原的H2SO4的物质的量是1__mol,浓硫酸表现的性质是酸性和强氧化性
(1)元素由化合态变为游离态,该元素不一定被还原
(2)在氧化还原反应中,一种元素被氧化,不一定有另一种元素被还原,也可能是同一元素既被氧化又被还原
氧化还原反应电子转移的表示方法(1)双线桥法:①标变价,②画箭头,③算数目,④说变化
实例:用双线桥法标出铜和浓硝酸反应电子转移的方向和数目
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得到”、“失去”字样
实例:用单线桥法标出铜和稀硝酸反应电子转移的方向和数目
氧化还原反应与四种基本反应类型的关系二、常见的氧化剂和还原剂1
常见氧化剂常见氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等
常见还原剂常见还原剂包括活泼的金属单质、非金属离子及低价态化合物、低价金属阳离子、非金属单质及其氢化物等
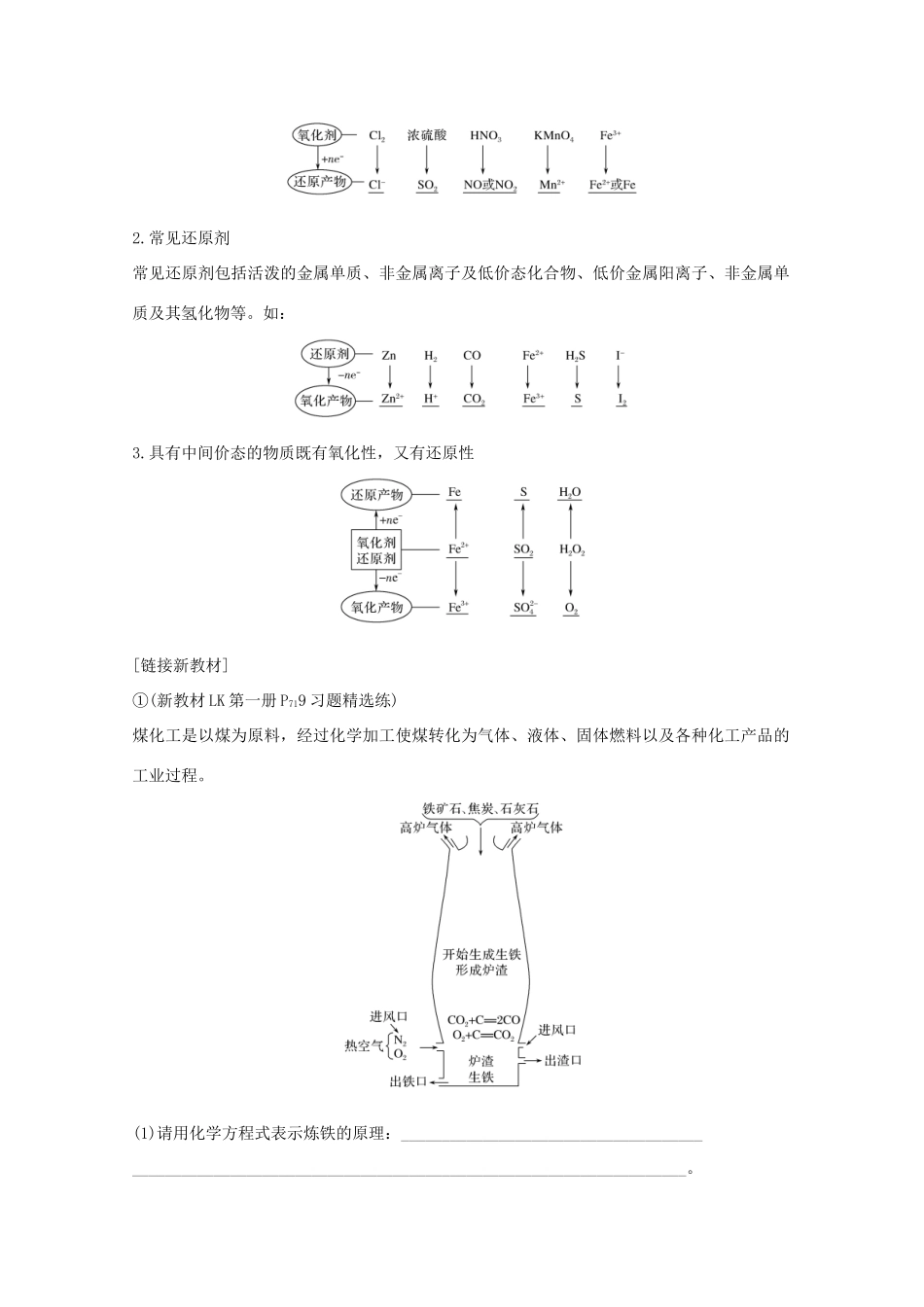
具有中间价态的物质既有氧化性,又有还原性[链接新教材]①(新教材LK第一册P719习题精选练)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化