第二节影响化学反应速率的因素目标与素养:1
理解外界条件(温度、浓度、压强、催化剂等)对化学反应速率的影响,认识其一般规律
(宏观辨识与科学探究)2
知道活化能的含义及其对化学反应速率的影响(宏观辨识与科学探究)3
了解催化剂在生产、生活和科学研究领域中的重大作用
(科学态度与社会责任)4
认识化学反应速率的调控在生活、生产和科学研究领域中的重要作用
(科学态度与社会责任)一、有效碰撞理论简介1.有效碰撞2.活化分子与活化能活化能越小,普通分子就越容易变成活化分子
如图所示:反应的活化能是E1,反应热是E1-E2
3.化学反应速率与活化分子、有效碰撞的关系活化分子的百分数越大,单位体积内活化分子数越多,单位时间内有效碰撞次数越多,化学反应速率越快
举例说明实现向体系提供活化能的方法有哪些
[答案]加热、光照、超声波、核辐射、研磨等
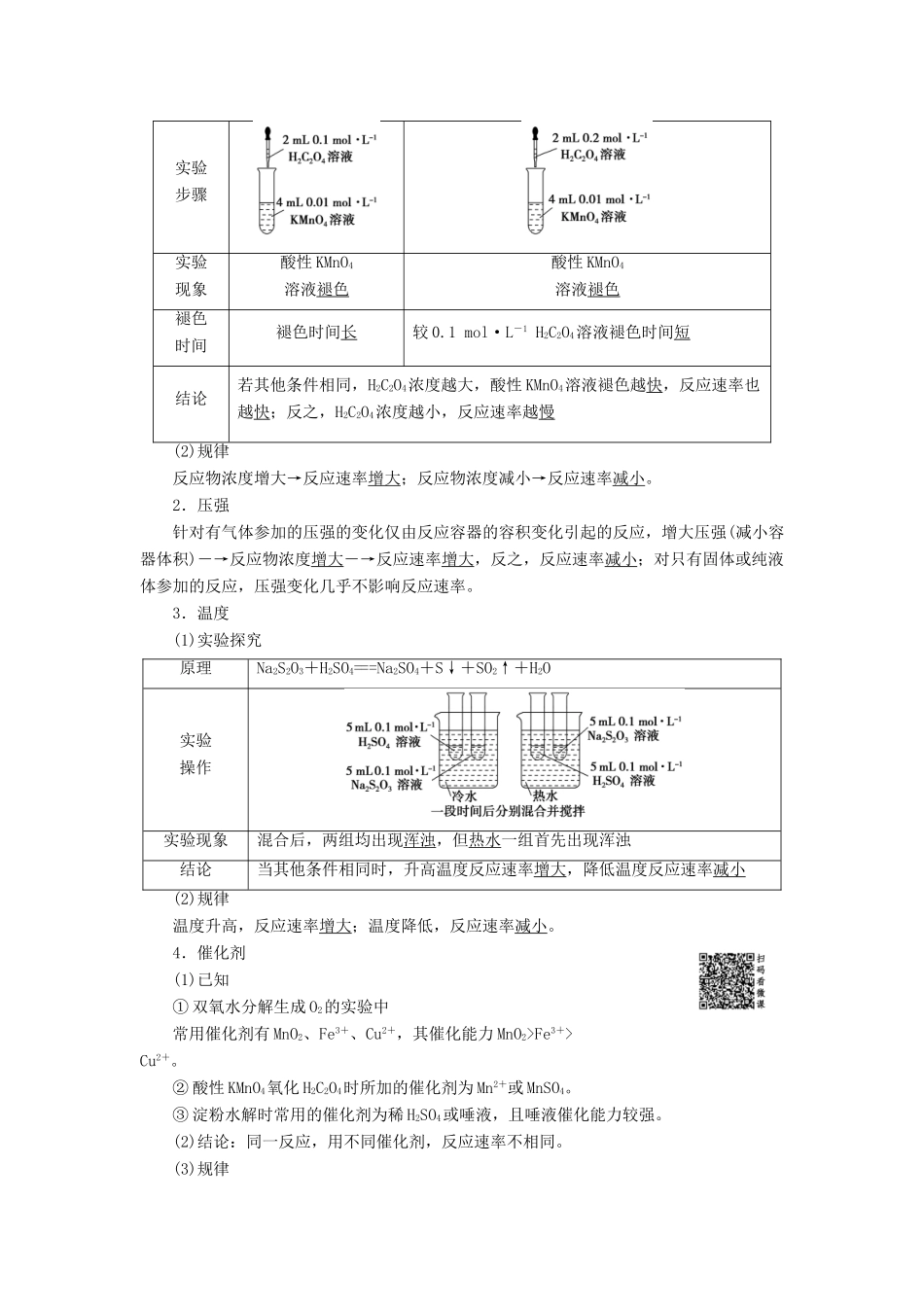
二、外界因素对化学反应速率的影响1.浓度(1)实验探究原理2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O实验步骤实验现象酸性KMnO4溶液褪色酸性KMnO4溶液褪色褪色时间褪色时间长较0
1mol·L-1H2C2O4溶液褪色时间短结论若其他条件相同,H2C2O4浓度越大,酸性KMnO4溶液褪色越快,反应速率也越快;反之,H2C2O4浓度越小,反应速率越慢(2)规律反应物浓度增大→反应速率增大;反应物浓度减小→反应速率减小
2.压强针对有气体参加的压强的变化仅由反应容器的容积变化引起的反应,增大压强(减小容器体积)―→反应物浓度增大―→反应速率增大,反之,反应速率减小;对只有固体或纯液体参加的反应,压强变化几乎不影响反应速率
3.温度(1)实验探究原理Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O实验操作实验现象混合后,两组均出现浑浊,但热水一组首先出现浑浊结论当其他条件相同时