酸碱中和滴定学习目标:1、理解酸碱中和滴定的原理
2、掌握有关酸碱中和滴定的实验及相关计算
3、理解滴定分析实验的关键所在及其解决方法学习重难点:酸碱中和滴定的原理和滴定分析实验的关键所在及其解决方法;酸碱中和滴定的计算依据及有关计算及误差分析
自主学习1、酸碱中和滴定概念:利用反应,用来测定的方法
2、酸碱中和滴定的原理:当酸碱恰好中和时,酸含有的的物质的量等于碱含有的的物质的量
若酸是n元酸,碱是m元碱,则C酸·V酸·n=C碱·V碱·m
我们常把已知浓度的酸(或碱)称为,将未知浓度的碱(或酸)称为
3、酸碱中和滴定需要使用滴定管,其主要用来,常见规格有和,读数时精确到ml
滴定管分为和两种,酸式滴定管只能用来装,碱式滴定管只能用来装
滴定管在使用的步骤是→→→→→→→
4、准确判断酸碱是否恰好中和,要选择合适的,借助指示剂明显的颜色变化来表示,颜色发生变化时该点称为,把酸碱恰好中和的最后一滴酸或碱引起溶液PH的突变叫酸碱中和滴定的突跃范围
5、滴定过程中的注意事项:⑴酸式滴定管应排走气泡,碱式滴定管应排走气泡
⑵标准溶液一般放在中留待滴定,待测溶液通过滴定管或移液管准确取出放在中
⑶滴定过程中,左手,右手、眼睛注视着,直到到达滴定终点,滴定速度
⑷滴定终点的现象是:
6、若用已知浓度的一元强酸滴定未知浓度的一元强碱,请写出计算公式:(碱)=7、误差分析(一元酸、碱的中和滴定):若标准溶液滴定待测溶液,标准液消耗多,则结果偏大;标准液消耗少,则结果偏低
读数引起的误差经常容易错,所以借助画图的形式能更好地理解和记忆:合作探究:1
什么是定性分析
什么是定量分析
中和滴定是定性还是定量分析
酸碱中和滴定过程中,使用酸碱指示剂要注意哪些地方
(用量和选择)⑴用量:酸碱指示剂本身就是一些,若过量会消耗滴定中的造成误差,所以一般加入滴即可
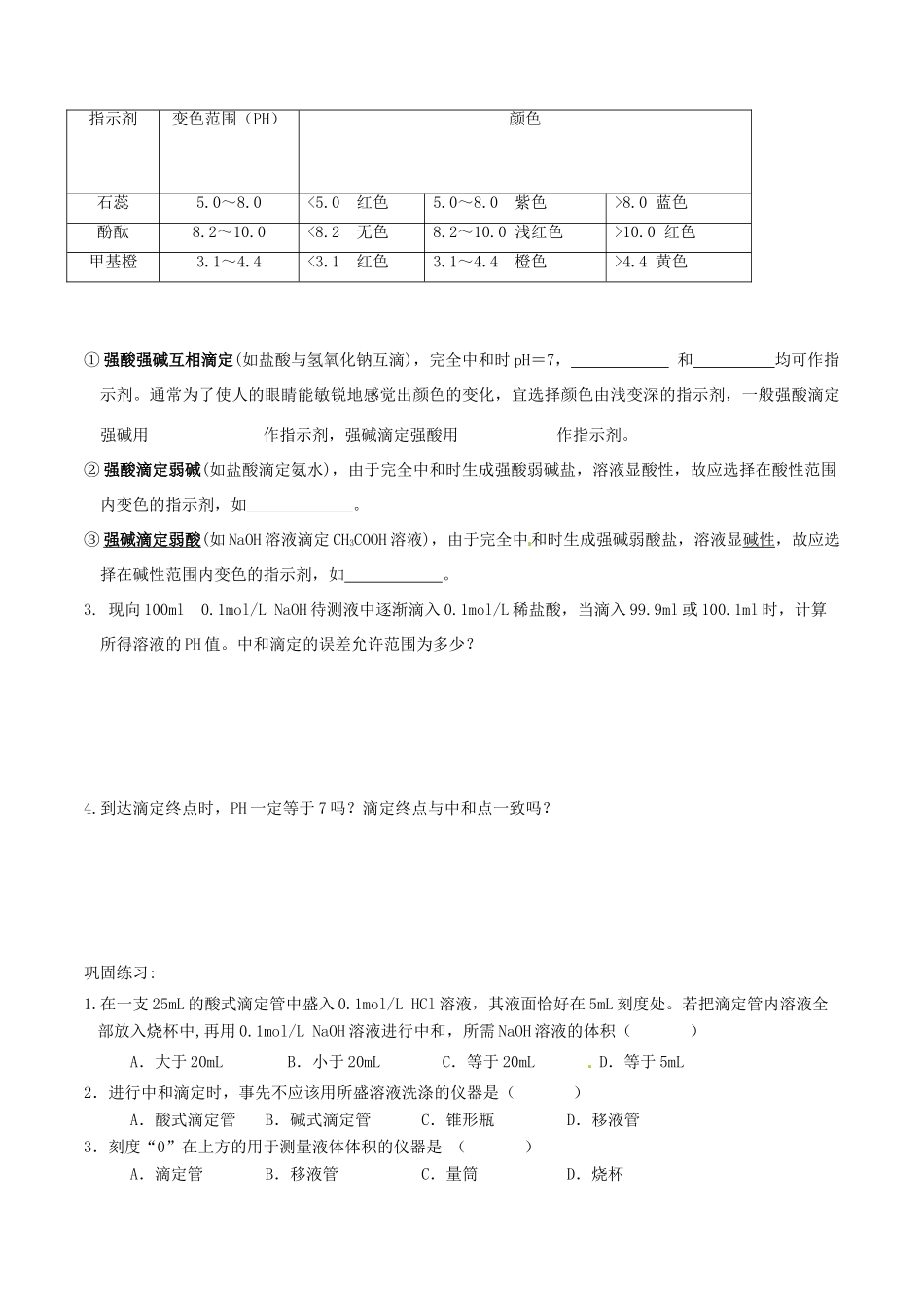
⑵高中阶段常见的酸碱指示剂有、、