第四节离子晶体1.能说明离子键的形成,能根据离子化合物的结构特征解释其物理性质
了解晶格能的应用,知道晶格能的大小可以衡量离子晶体中离子键的强弱
知道离子晶体的结构微粒、微粒间作用力以及与其他晶体的区别
离子晶体1.结构特点(1)构成粒子:阳离子和阴离子
(2)作用力:离子键
(3)配位数:一个离子周围最邻近的异电性离子的数目
2.结构的决定因素(1)几何因素:晶体中正负离子的半径比
(2)电荷因素:晶体中正负离子的电荷比
(3)键性因素:离子键的纯粹程度
3.性质熔、沸点熔、沸点较高,难挥发硬度硬度较大,难于压缩溶解性一般在水中易溶,在非极性溶剂中难溶导电性固态时不导电,熔融状态或在水溶液中能导电4
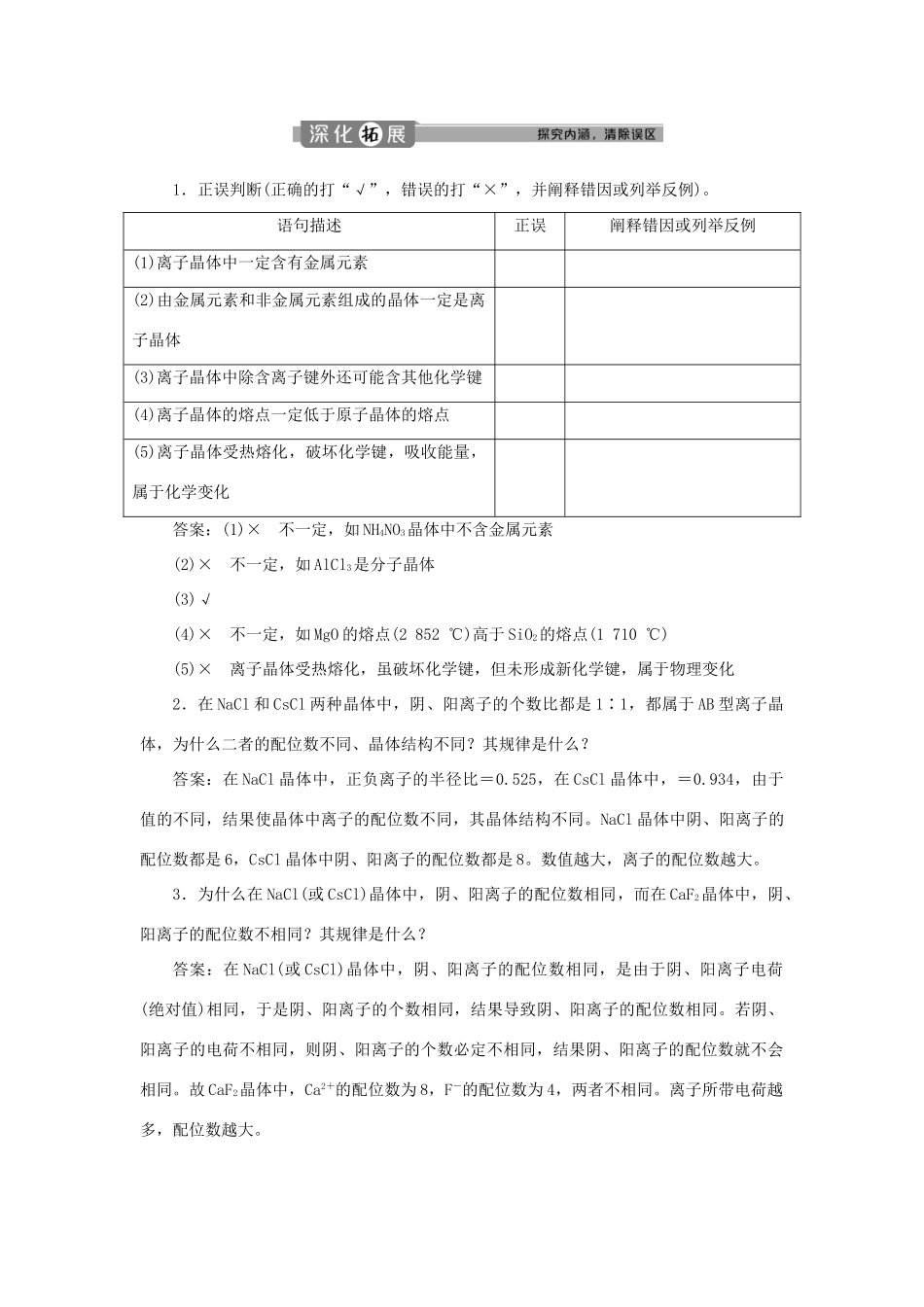
常见的离子晶体NaClCsClCaF2晶胞阴离子的配位数684阳离子的配位数6881.正误判断(正确的打“√”,错误的打“×”,并阐释错因或列举反例)
语句描述正误阐释错因或列举反例(1)离子晶体中一定含有金属元素(2)由金属元素和非金属元素组成的晶体一定是离子晶体(3)离子晶体中除含离子键外还可能含其他化学键(4)离子晶体的熔点一定低于原子晶体的熔点(5)离子晶体受热熔化,破坏化学键,吸收能量,属于化学变化答案:(1)×不一定,如NH4NO3晶体中不含金属元素(2)×不一定,如AlCl3是分子晶体(3)√(4)×不一定,如MgO的熔点(2852℃)高于SiO2的熔点(1710℃)(5)×离子晶体受热熔化,虽破坏化学键,但未形成新化学键,属于物理变化2.在NaCl和CsCl两种晶体中,阴、阳离子的个数比都是1∶1,都属于AB型离子晶体,为什么二者的配位数不同、晶体结构不同
其规律是什么
答案:在NaCl晶体中,正负离子的半径比=0
525,在CsCl晶体中,=0
934,由于值的不同,结果使晶体中离子的配位数不同,其晶体结构不同
NaCl晶体中阴、阳离子的配位数都是6