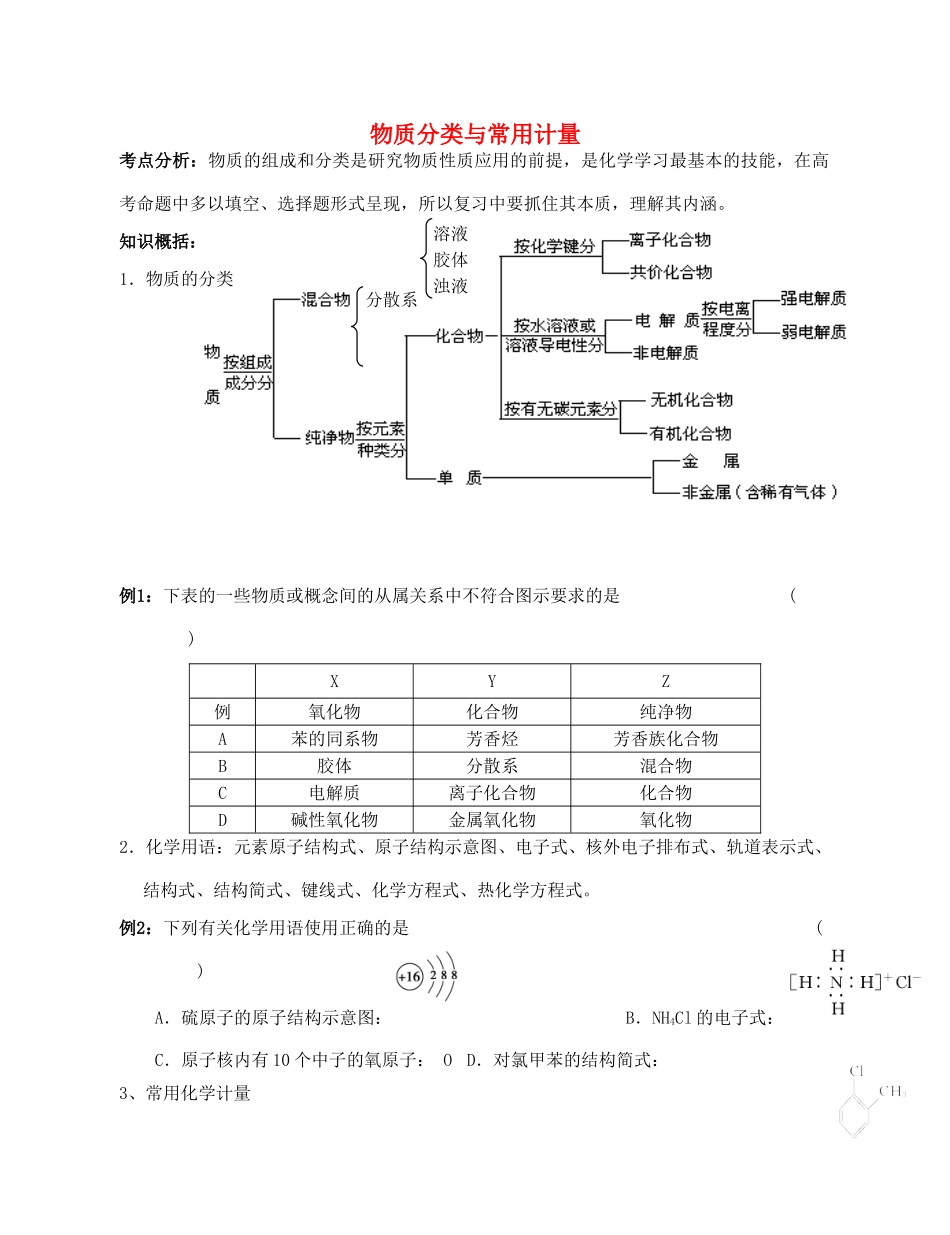
物质分类与常用计量考点分析:物质的组成和分类是研究物质性质应用的前提,是化学学习最基本的技能,在高考命题中多以填空、选择题形式呈现,所以复习中要抓住其本质,理解其内涵
知识概括:1.物质的分类例1:下表的一些物质或概念间的从属关系中不符合图示要求的是()XYZ例氧化物化合物纯净物A苯的同系物芳香烃芳香族化合物B胶体分散系混合物C电解质离子化合物化合物D碱性氧化物金属氧化物氧化物2.化学用语:元素原子结构式、原子结构示意图、电子式、核外电子排布式、轨道表示式、结构式、结构简式、键线式、化学方程式、热化学方程式
例2:下列有关化学用语使用正确的是()A.硫原子的原子结构示意图:B.NH4Cl的电子式:C.原子核内有10个中子的氧原子:OD.对氯甲苯的结构简式:3、常用化学计量分散系溶液胶体浊液例3:用NA表示阿伏加德罗常数的值
下列叙述正确的是()A.17g甲基(—14CH3)所含中子数为9NAB.标准状况下,密度为ρg·L-1的某气体纯净物一个分子的质量为gC.25℃时,1LpH=13的NaOH溶液中含有NA个氢氧根离子D.常温下,0
2molCl2溶于等体积水中,转移电子数为0
2NA例4:在t℃时,将agNH3完全溶于水,得到VmL溶液,假设该溶液的密度为ρg·cm-3,质量分数为w,其中含NH4+的物质的量为bmol
下列叙述中正确的是()A.溶质的质量分数为w=×100%B.溶质的物质的量浓度c=mol·L-1C.溶液中c(OH-)=mol·L-1+c(H+)D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0
5c实战演练:一、选择题1.“化学是人类进步的关键”
下列有关说法能反映正确化学观点的是(×22
4(L/mol)÷22
4(L/mol)×V÷V÷NA÷M物质的量(mol)×NA微粒数N质量(g)×M物质的量浓度(mol/L)标况下气体体积(L))A.改