第一节弱电解质的电离学习目标1
能描述弱电解质在水溶液中的电离平衡,了解酸碱电离理论;2
了解电离平衡常数及其意义;3
了解强电解质和弱电解质与其结构的关系
学习过程【复习提问】1
电解质、非电解质的概念
为什么电解质在水溶液里或熔融状态下能够导电
一、强弱电解质【实验探究】分别试验等体积、等浓度的盐酸、醋酸溶液与等量镁条反应;并测这两种酸的pH
1mol·L-1HCl1mol·L-1CH3COOH与镁条反应的现象溶液的pH结论【交流研讨1】1
为什么相同浓度的盐酸和醋酸中的H+浓度不同
如何理解醋酸的部分电离
(已知信息:向醋酸溶液中加入CH3COONH4固体,溶液的H+浓度变小
盐酸的电离也有电离平衡吗
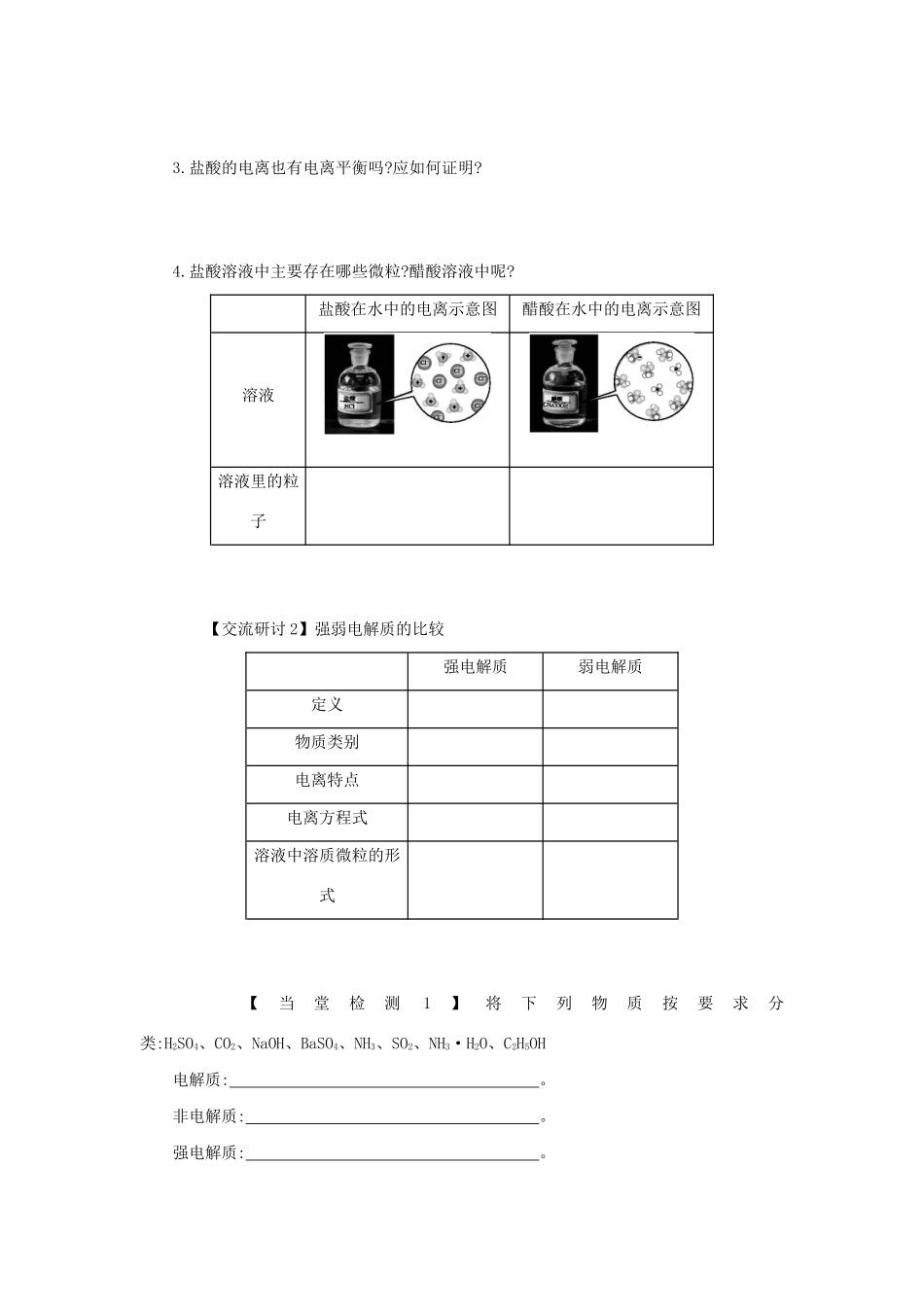
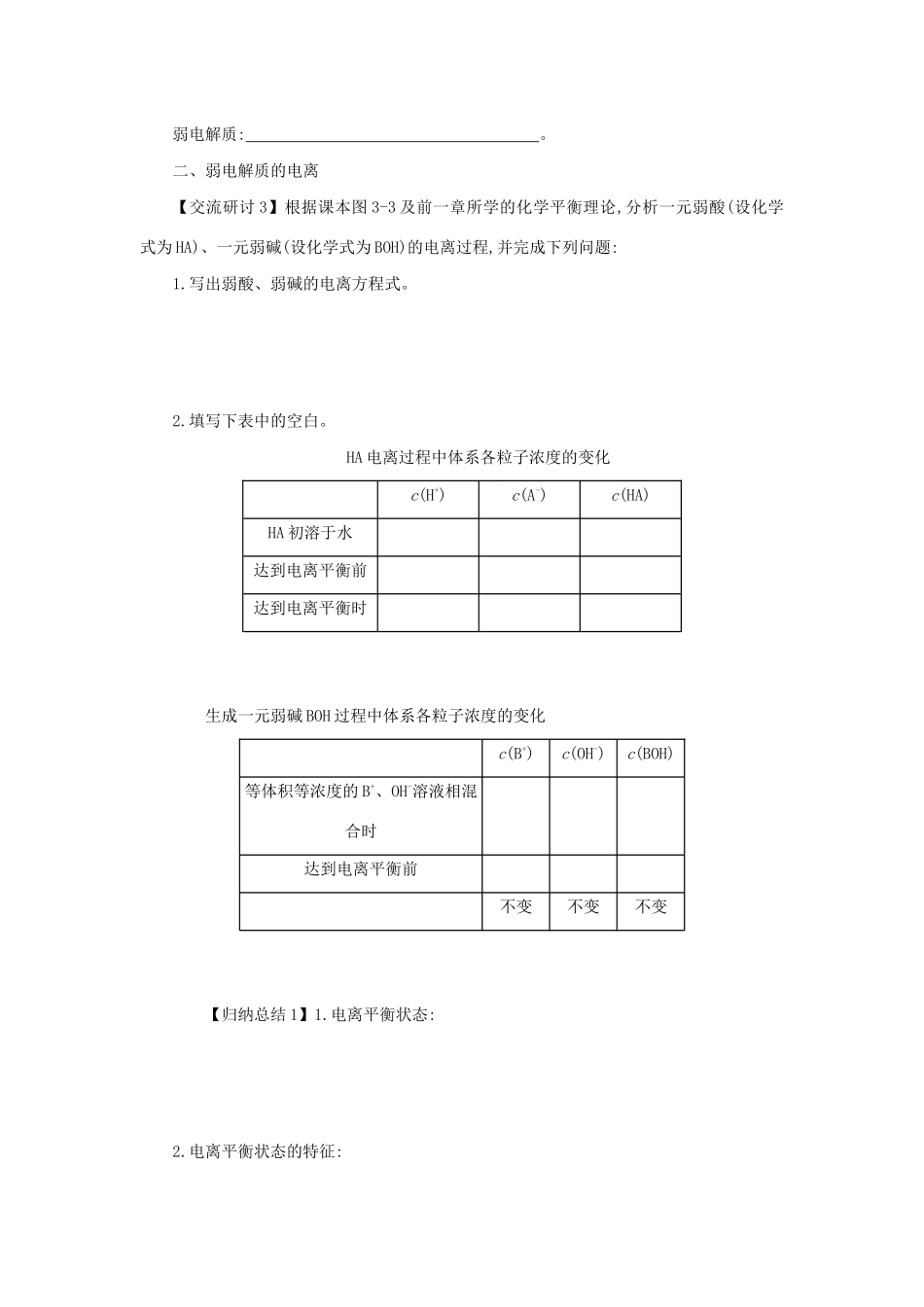
盐酸溶液中主要存在哪些微粒
醋酸溶液中呢
盐酸在水中的电离示意图醋酸在水中的电离示意图溶液溶液里的粒子【交流研讨2】强弱电解质的比较强电解质弱电解质定义物质类别电离特点电离方程式溶液中溶质微粒的形式【当堂检测1】将下列物质按要求分类:H2SO4、CO2、NaOH、BaSO4、NH3、SO2、NH3·H2O、C2H5OH电解质:
二、弱电解质的电离【交流研讨3】根据课本图3-3及前一章所学的化学平衡理论,分析一元弱酸(设化学式为HA)、一元弱碱(设化学式为BOH)的电离过程,并完成下列问题:1
写出弱酸、弱碱的电离方程式
填写下表中的空白
HA电离过程中体系各粒子浓度的变化c(H+)c(A-)c(HA)HA初溶于水达到电离平衡前达到电离平衡时生成一元弱碱BOH过程中体系各粒子浓度的变化c(B+)c(OH-)c(BOH)等体积等浓度的B+、OH-溶液相混合时达到电离平衡前不变不变不变【归纳总结1】1
电离平衡状态:2
电离平衡状态的特征:【当堂检测2】请写出下列电解质的电离方程式:(1)NH3·H2O: