第3课时硝酸人类活动对氮循环和环境的影响发展目标体系构建1
通过对硝酸性质的学习,认识硝酸的物理性质、化学性质以及典型实验现象,能书写主要反应的化学方程式,知道他们的主要应用;建立从物质类别、元素价态角度实现含有氮元素的物质之间转化的思想和方法
通过人类对氮循环的影响,了解酸雨、光化学烟雾和富营养化等环境问题的危害以及如何减少氮氧化物的排放,树立环保意识,同时知道常见氮的化合物在实验室中的安全使用注意事项
能够预测陌生的含有氮元素物质的性质、反应或实验现象,设计方案制备含有氮元素的物质和研究他们的性质
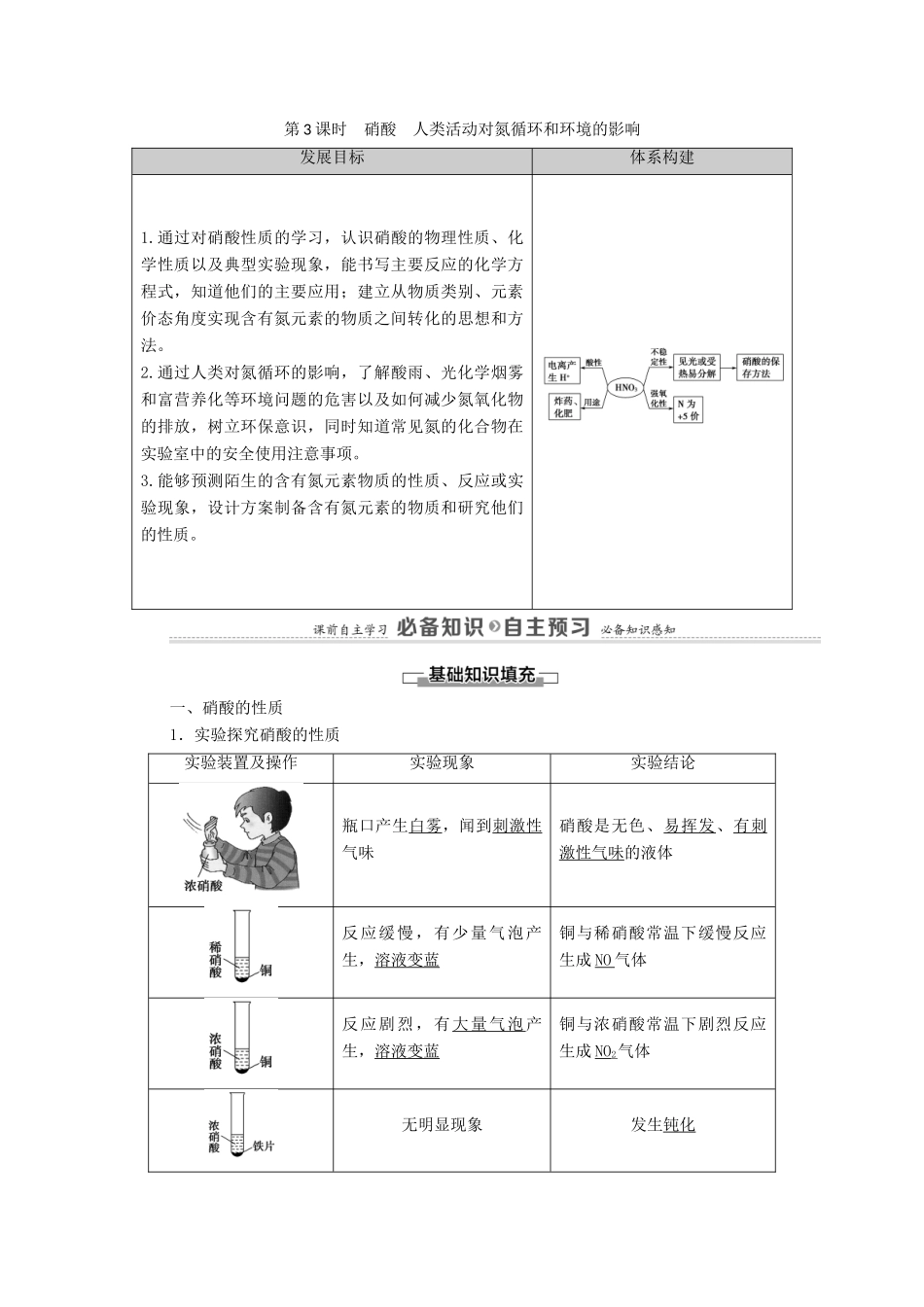
一、硝酸的性质1.实验探究硝酸的性质实验装置及操作实验现象实验结论瓶口产生白雾,闻到刺激性气味硝酸是无色、易挥发、有刺激性气味的液体反应缓慢,有少量气泡产生,溶液变蓝铜与稀硝酸常温下缓慢反应生成NO气体反应剧烈,有大量气泡产生,溶液变蓝铜与浓硝酸常温下剧烈反应生成NO2气体无明显现象发生钝化2
物理性质颜色状态气味密度特性无色液态刺激性ρHNO3>ρH2O易挥发3
化学性质(1)酸的通性:电离方程式为HNO3===H++NO
硝酸能使酸碱指示剂发生颜色变化,能与金属、碱、碱性氧化物等反应
(2)不稳定性:浓硝酸受热或见光分解,化学方程式为4HNO3=====4NO2↑+O2↑+2H2O
(3)强氧化性:4.用途硝酸是一种重要的化工原料,可用于制造炸药、染料等,也是实验室里重要的化学试剂
二、人类活动对氮循环和环境的影响1.氮氧化物与碳氢化合物发生反应产生光化学烟雾
2.氮氧化物还是雾霾的主要成分之一
3.氮氧化物与水反应生成硝酸和亚硝酸,形成酸雨
4.工业废水和农业废水排放造成水体富营养化
1.判断正误(正确的打“√”,错误的打“×”)
(1)常温下铁与浓硝酸反应,产生大量红棕色气体
()(2)用浓硝酸与Cu反应制备NO2
()(3)碳与硝酸在常温下即可反应