第12讲铜及其重要化合物、金属材料一、铜及其化合物1.铜的性质(1)物理性质:铜是□紫红色金属,具有良好的□导电性、□导热性和延展性
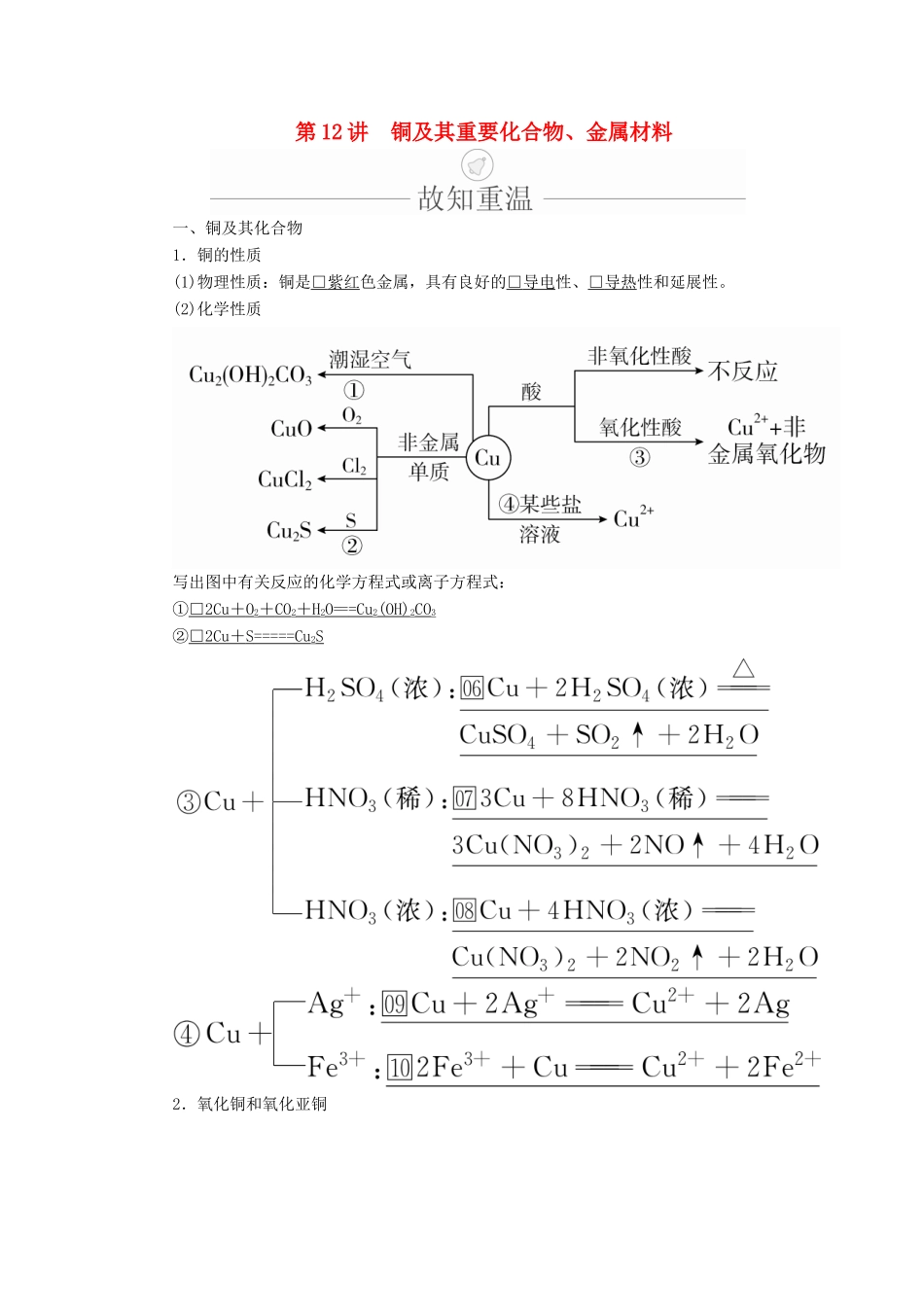
(2)化学性质写出图中有关反应的化学方程式或离子方程式:①□2Cu+O2+CO2+H2O===Cu2(OH)2CO3②□2Cu+S=====Cu2S2.氧化铜和氧化亚铜3.氢氧化铜(1)物理性质:□蓝色□不溶于水的固体
(2)化学性质及应用4.CuSO4·5H2OCuSO4·5H2O为□蓝色晶体,俗称□蓝矾、胆矾
无水CuSO4为□白色粉末,遇水变蓝色(生成CuSO4·5H2O),可作为水的检验依据
无水CuSO4只能作为水的检验试剂,但不能作为水蒸气的吸收试剂而用于除杂
二、金属材料1.合金2.常见金属材料(1)黑色金属材料——钢铁
①□钢是用量最大,用途最广的合金
(2)有色金属材料——铜和铝
①我国使用最早的合金是□青铜,常见的铜合金有黄铜和白铜等
②铝合金3.金属矿物的开发利用(1)金属在自然界中的存在(2)金属冶炼的一般步骤(3)金属冶炼的实质金属的冶炼过程就是把金属从□化合态还原为□游离态的过程
即□Mn++ne-=M
(4)金属冶炼的方法(用化学方程式表示)1
判断正误,正确的画“√”,错误的画“×”,并指明错因
(1)除去Cu粉中混有CuO的方法是加入稀硝酸溶解、过滤、洗涤、干燥
(×)错因:Cu与HNO3也反应
(2)将铜粉加入1
0mol·L-1Fe2(SO4)3溶液中,现象是溶液变蓝,有黑色固体出现
(×)错因:Fe3+氧化铜,本身被还原为Fe2+,没有黑色固体生成
(3)1molCu和足量热浓硫酸反应可生成NA个SO3分子
(×)错因:Cu与热浓H2SO4反应产生SO2
(4)合金中的金属元素都是以化合态形式存在
(×)错因:合金中金属多是以游离态形式存在的
(5)合金的硬度一般小于成分金属,而熔点一般高于成分金属