第10讲镁、铝及其重要化合物一、镁及其重要化合物的主要性质和应用1.镁的性质(1)物理性质:具有□银白色金属光泽的固体,密度、硬度均较□小,熔点较□低,有良好的□导电性、□导热性和□延展性
(2)化学性质①与非金属反应②与CO2反应:□2Mg+CO2=====2MgO+C③与H2O反应:□Mg+2H2O=====Mg(OH)2+H2↑④与H+反应:□Mg+2H+===Mg2++H2↑2.从海水中提取镁的流程(1)流程(2)主要化学反应①制石灰乳□CaCO3=====CaO+CO2↑、□CaO+H2O===Ca(OH)2;②沉淀Mg2+:□Mg2++Ca(OH)2===Mg(OH)2↓+Ca2+;③制备MgCl2:□Mg(OH)2+2HCl===MgCl2+2H2O;④电解MgCl2:□MgCl2(熔融)=====Mg+Cl2↑
3.用途生产□合金,冶金工业上用作□还原剂和□脱氧剂
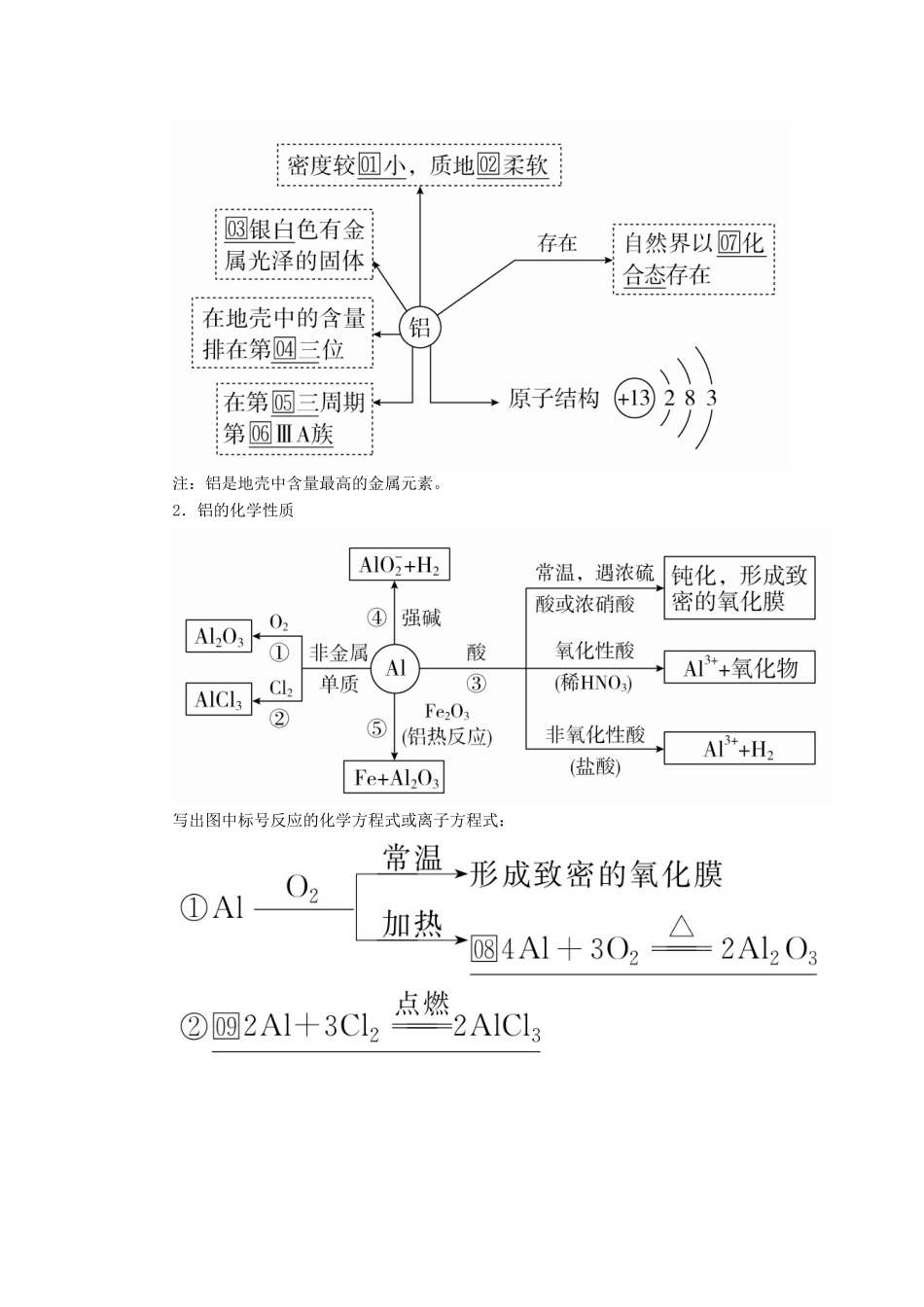
4.镁的重要化合物二、铝的性质及应用1.铝的物理性质注:铝是地壳中含量最高的金属元素
2.铝的化学性质写出图中标号反应的化学方程式或离子方程式:④□2Al+2OH-+2H2O===2AlO+3H2↑⑤□2Al+Fe2O3=====Al2O3+2Fe(铝热反应)3.铝的制备及用途三、铝的重要化合物1.氧化铝(1)物理性质:白色固体,难溶于水,有很高的熔点
(2)化学性质2.氢氧化铝(1)物理性质白色胶状不溶于水的固体,有较强的□吸附性
(2)化学性质(用化学方程式表示)Al(OH)3的电离方程式为②受热分解:□2Al(OH)3=====Al2O3+3H2O
(3)制备①向铝盐中加入氨水,离子方程式为Al3++3NH3·H2O===Al(OH)3↓+3NH
②向NaAlO2溶液中通入足量CO2,离子方程式为AlO+CO2+2H2O===Al(OH)3↓+HCO
③NaAlO2溶液与AlCl3溶液混合: