第二节原子结构与元素的性质第二课时【学习目标】1
掌握原子半径的变化规律2
能说出元素电离能的涵义,能应用元素的电离能说明元素的某些性质3
进一步形成有关物质结构的基本观念,初步认识物质的结构与性质之间的关系4
认识主族元素电离能的变化与核外电子排布的关系5
认识原子结构与元素周期系的关系,了解元素周期系的应用价值【学习过程】【课前预习】1
气态原子或离子叫电离能,常用符号表示,单位为叫第一电离能
根据电离能的定义可知,电离能越小,表示在气态时该原子,反之,电离能越大,表示在气态时该原子,同一周期从左到右,元素的第一电离能总体上具有的趋势,同一主族从上到下,第一电离能
【知识梳理】二、元素周期律(1)原子半径〖探究〗观察下列图表分析总结:元素周期表中同周期主族元素从左到右,原子半径的变化趋势如何
应如何理解这种趋势
元素周期表中,同主族元素从上到下,原子半径的变化趋势如何
应如何理解这种趋势
【归纳总结】(2)电离能1
第一电离能I1:态电性基态原子失去个电子,转化为气态基态正离子所需要的叫做第一电离能
第一电离能越大,金属活动性越
同一元素的第二电离能第一电离能
如何理解第二电离能I2、第三电离能I3、I4、I5……
分析下表:【思考总结】1、原子的第一电离能有什么变化规律呢
碱金属元素的第一电离能有什么变化规律呢
为什么Be的第一电离能大于B,N的第一电离能大于O,Mg的第一电离能大于Al,Zn的第一电离能大于Ga
第一电离能的大小与元素的金属性和非金属性有什么关系
碱金属的电离能与金属活泼性有什么关系
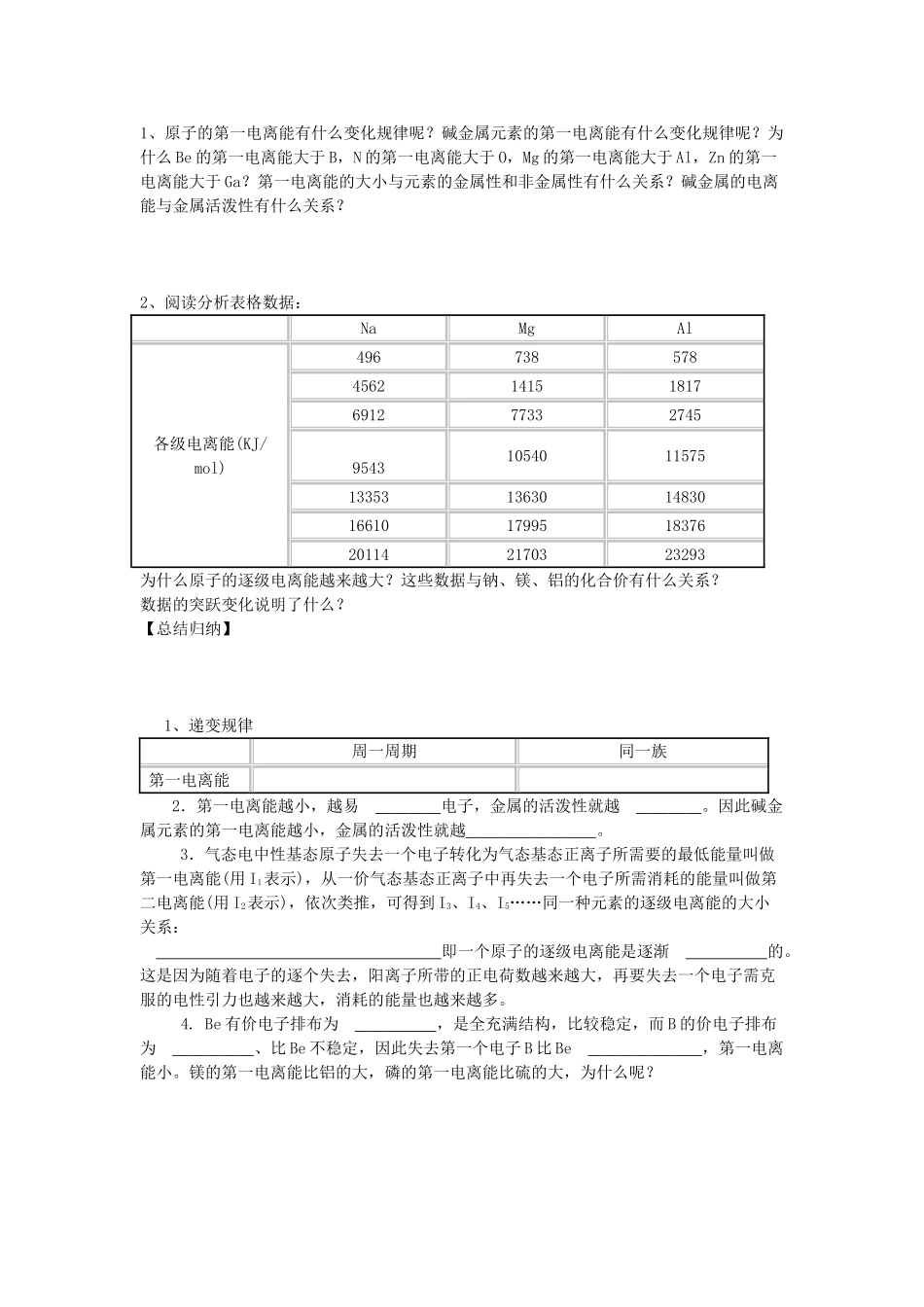
2、阅读分析表格数据:NaMgAl各级电离能(KJ/mol)49673857845621415181769127733274595431054011575133531363014830166101799518376201142170323293为什么原子的逐级电