第5课时化学平衡图像学习目标理解化学平衡图像的意义,掌握化学平衡图像题的解法
学习过程一、解题思路(1)看懂图像面:图像形状,横、纵坐标的含义;线:走向,变化趋势;点:起点、终点、交点、拐点;是否需作辅助线(等温线、等压线)来定量分析图像中有关量的多少
(2)联想规律,作出判断①浓度、压强、温度、加都可以使速率增大
②增加反应物浓度,减少生成物浓度,向反应方向移动,增大压强,向反应方向移动,升高温度,向反应方向移动
二、典型的化学平衡图像【课内探究】1
物质的量(或浓度)—时间图像【例1】某温度下,A、B、C三种物质的浓度随着时间变化的关系如图所示,则:(1)该反应的化学方程式为
(2)A、B的转化率分别为
【跟踪练习1】已知NO2和N2O4可以相互转化:2NO2(g)N2O4(g)(正反应为放热反应)
现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图所示,回答下列问题:(1)图中共有两条曲线X和Y,其中曲线表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是
(2)前10min内用NO2表示的化学反应速率v(NO2)=mol·L-1·min-1;反应进行至25min时,曲线发生变化的原因是
(3)若要达到与最后相同的化学平衡状态,在25min时还可以采取的措施是
加入催化剂B
缩小容器体积C
加入一定量的N2O42
速率—时间图像【例2】观察下列图像特点,并描述出改变平衡的条件分别是什么
下述图像的特点是:有一速率是改变的,另一速率是改变的
这是改变引起化学平衡移动的特征
【跟踪练习2】下述图线的特点是:正、逆反应速率都是改变的,且改变的不同
这是改变和引起化学平衡移动的特征
若或,都突然增大,若或,都突然减小
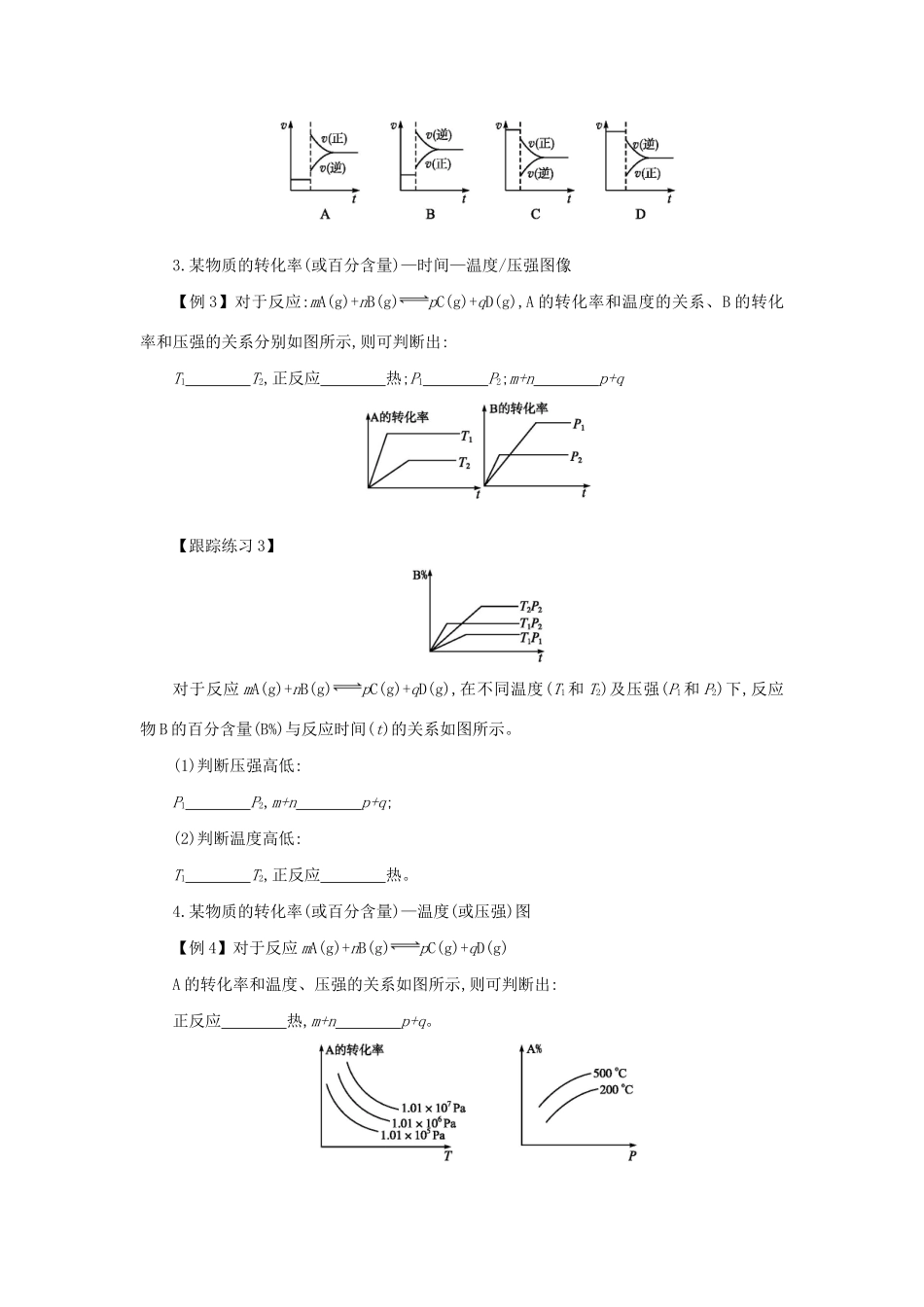
某物质的转化率(或百分含量)—时间—温度/压强图像【例3】对于