第七章化学反应速率化学平衡[考纲解读]1
了解化学反应速率的概念、反应速率的定量表示方法
能正确计算化学反应的转化率(α)
了解反应活化能的概念,了解催化剂的重要作用
了解化学反应的可逆性及化学平衡的建立
掌握化学平衡的特征
了解化学平衡常数(K)的含义
能利用化学平衡常数进行相关计算
理解外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,能用相关理论解释其一般规律
了解化学反应速率和化学平衡的调控在生产、生活和科学研究领域中的重要作用
第21讲化学反应速率1
化学反应速率2.化学反应速率的影响因素(1)内因(根本因素)反应物本身的□性质
(2)外因(其他条件不变,只改变一个条件)(3)理论解释——有效碰撞理论①活化分子、活化能、有效碰撞a.活化分子:能够发生□有效碰撞的分子
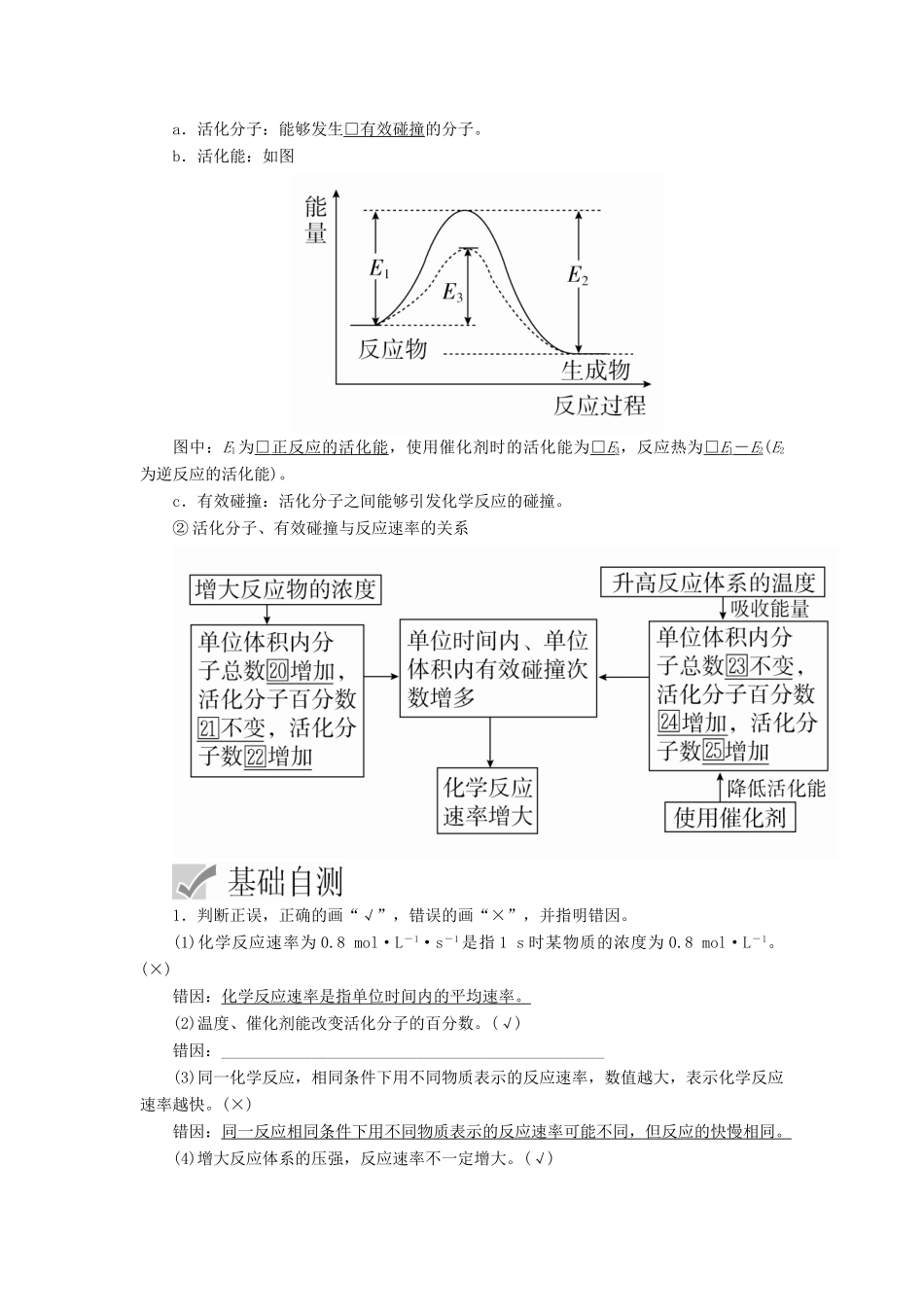
b.活化能:如图图中:E1为□正反应的活化能,使用催化剂时的活化能为□E3,反应热为□E1-E2(E2为逆反应的活化能)
c.有效碰撞:活化分子之间能够引发化学反应的碰撞
②活化分子、有效碰撞与反应速率的关系1.判断正误,正确的画“√”,错误的画“×”,并指明错因
(1)化学反应速率为0
8mol·L-1·s-1是指1s时某物质的浓度为0
8mol·L-1
(×)错因:化学反应速率是指单位时间内的平均速率
(2)温度、催化剂能改变活化分子的百分数
(√)错因:_______________________________________________(3)同一化学反应,相同条件下用不同物质表示的反应速率,数值越大,表示化学反应速率越快
(×)错因:同一反应相同条件下用不同物质表示的反应速率可能不同,但反应的快慢相同
(4)增大反应体系的压强,反应速率不一定增大
(√)错因:______________________________________________