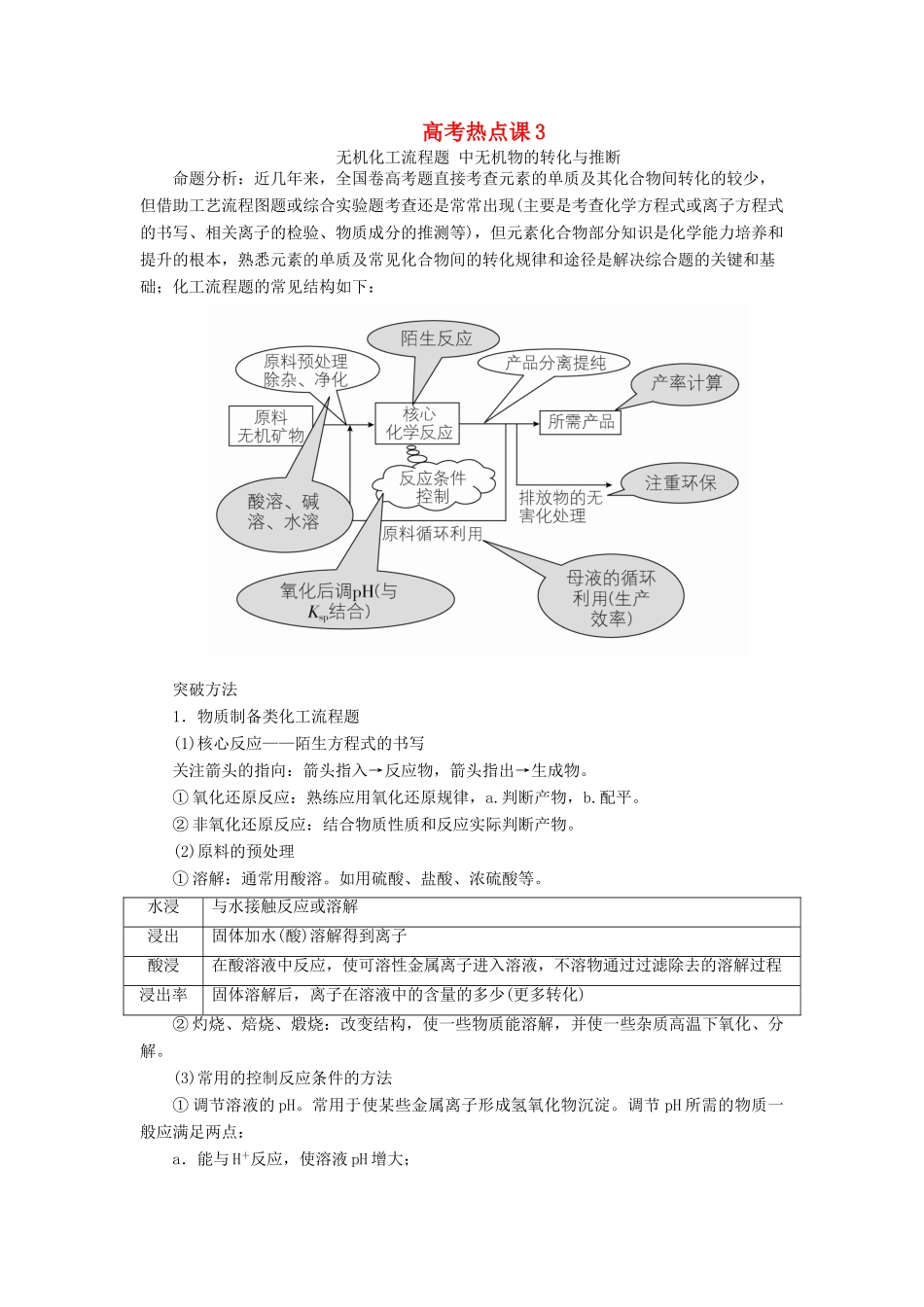
高考热点课3无机化工流程题中无机物的转化与推断命题分析:近几年来,全国卷高考题直接考查元素的单质及其化合物间转化的较少,但借助工艺流程图题或综合实验题考查还是常常出现(主要是考查化学方程式或离子方程式的书写、相关离子的检验、物质成分的推测等),但元素化合物部分知识是化学能力培养和提升的根本,熟悉元素的单质及常见化合物间的转化规律和途径是解决综合题的关键和基础;化工流程题的常见结构如下:突破方法1.物质制备类化工流程题(1)核心反应——陌生方程式的书写关注箭头的指向:箭头指入→反应物,箭头指出→生成物
①氧化还原反应:熟练应用氧化还原规律,a
判断产物,b
②非氧化还原反应:结合物质性质和反应实际判断产物
(2)原料的预处理①溶解:通常用酸溶
如用硫酸、盐酸、浓硫酸等
水浸与水接触反应或溶解浸出固体加水(酸)溶解得到离子酸浸在酸溶液中反应,使可溶性金属离子进入溶液,不溶物通过过滤除去的溶解过程浸出率固体溶解后,离子在溶液中的含量的多少(更多转化)②灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质高温下氧化、分解
(3)常用的控制反应条件的方法①调节溶液的pH
常用于使某些金属离子形成氢氧化物沉淀
调节pH所需的物质一般应满足两点:a.能与H+反应,使溶液pH增大;b.不引入新杂质
例如:若要除去Cu2+中混有的Fe3+,可加入CuO、CuCO3、Cu(OH)2、Cu2(OH)2CO3等物质来调节溶液的pH,不可加入NaOH溶液、氨水等
根据需要升温或降温,改变反应速率或使平衡向需要的方向移动
防止某物质降温时会析出
洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗
(2018·全国卷Ⅰ节选)焦亚硫酸钠(Na2S2O5)在医药、橡胶、印染、食品等方面应用广泛
回答下列问题:(1)生产Na2S2O5,通常是由NaHSO3