第11讲铁及其重要化合物一、铁的存在与性质1.铁在自然界中的存在形态:□游离态和化合态
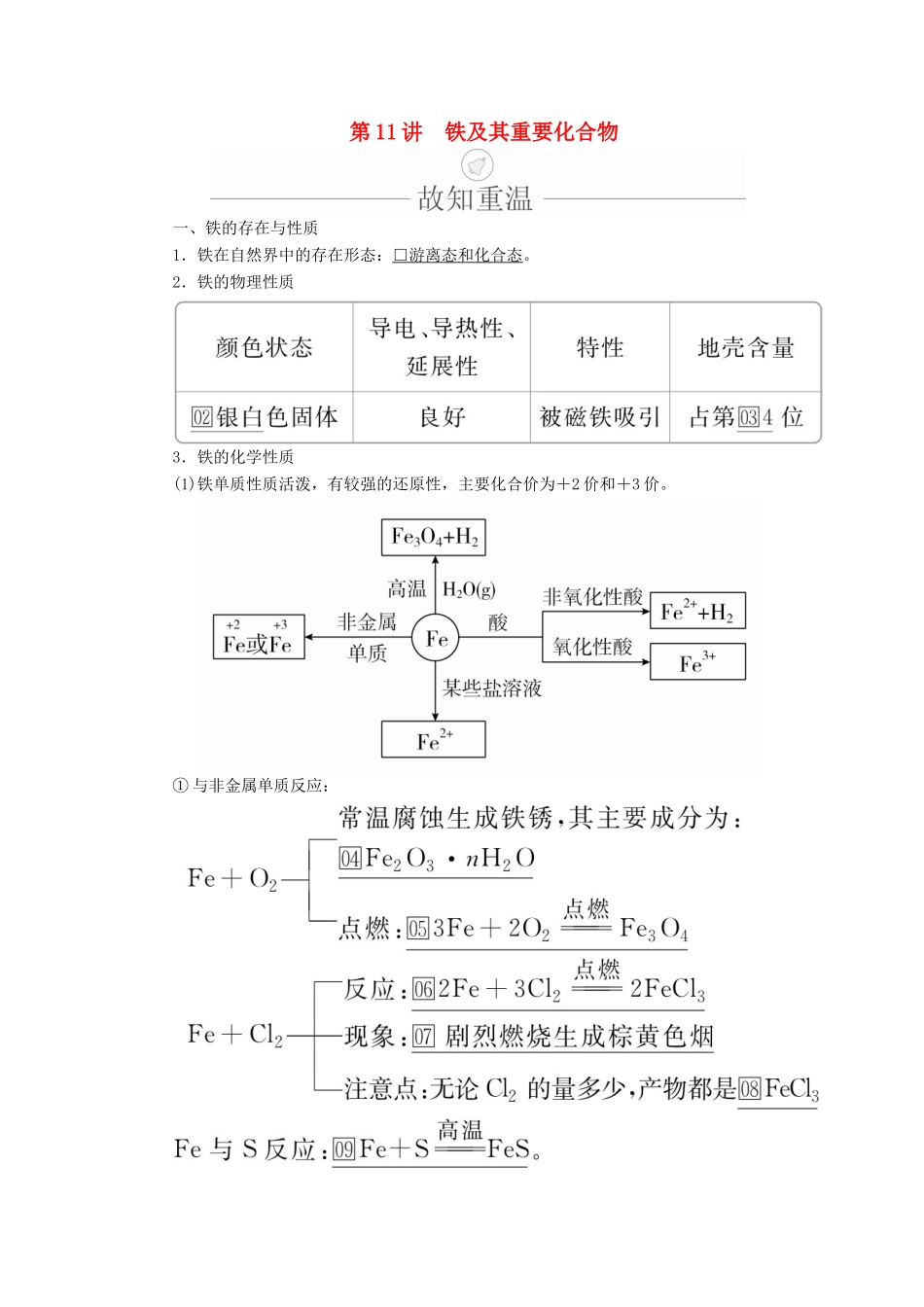
2.铁的物理性质3.铁的化学性质(1)铁单质性质活泼,有较强的还原性,主要化合价为+2价和+3价
①与非金属单质反应:②与水的反应:常温下铁与水不反应,在高温条件下与水蒸气反应:□3Fe+4H2O(g)=====Fe3O4+4H2
(2)与酸的反应(3)与某些盐溶液的反应①与CuSO4溶液反应的离子方程式:□Fe+Cu2+===Fe2++Cu
②与FeCl3溶液反应的离子方程式:□2Fe3++Fe===3Fe2+
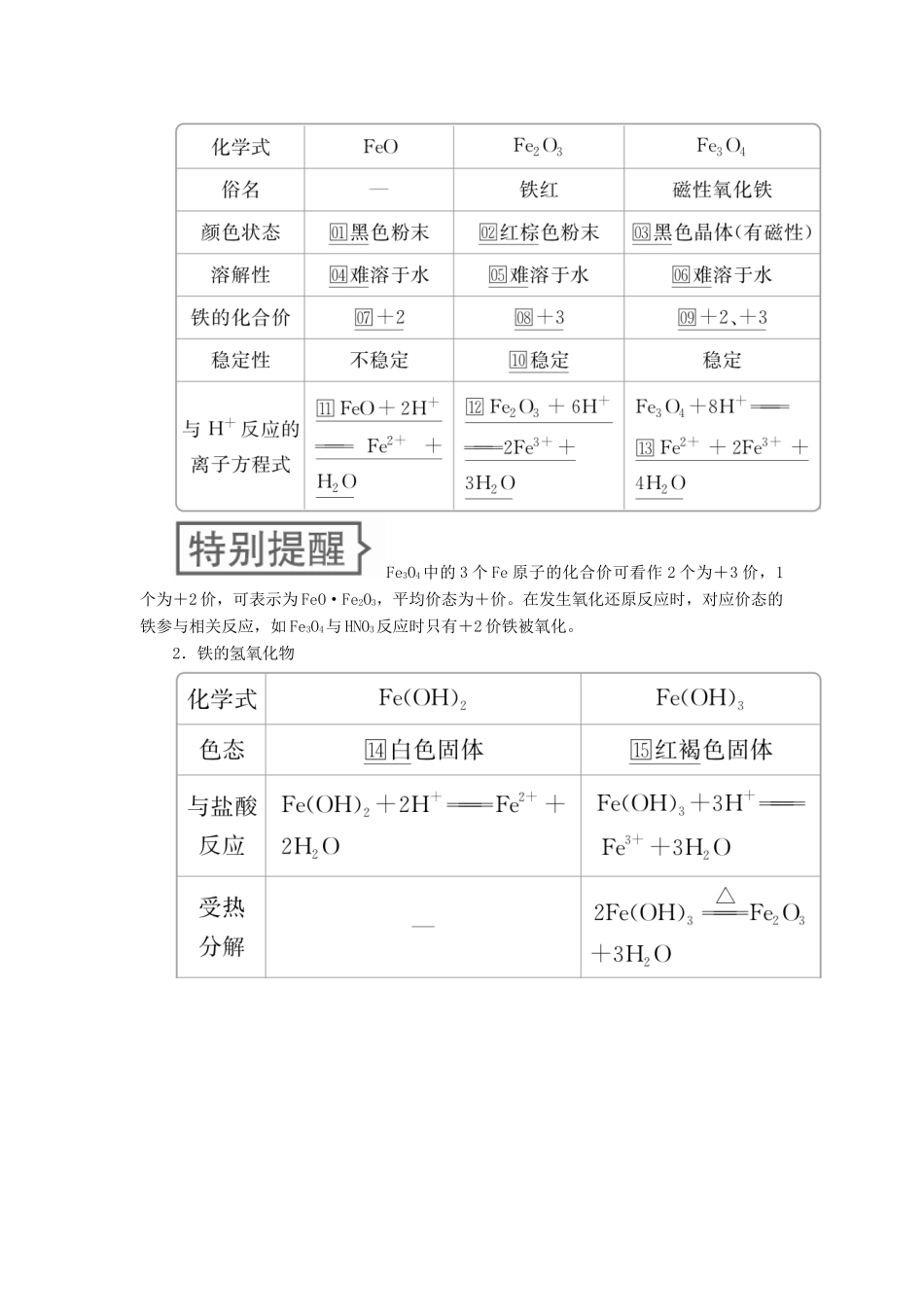
二、铁的氧化物和氢氧化物1.铁的氧化物Fe3O4中的3个Fe原子的化合价可看作2个为+3价,1个为+2价,可表示为FeO·Fe2O3,平均价态为+价
在发生氧化还原反应时,对应价态的铁参与相关反应,如Fe3O4与HNO3反应时只有+2价铁被氧化
2.铁的氢氧化物三、亚铁盐、铁盐的化学性质1.亚铁盐含有Fe2+的溶液呈□浅绿色,既有氧化性,又有还原性
(1)氧化性:Fe2+与Zn反应的离子方程式:□Zn+Fe2+===Fe+Zn2+
(2)还原性①向FeCl2溶液中滴入几滴KSCN溶液,再加入氯水(或通入Cl2),若溶液变红色,证明Fe2+具有还原性
反应原理:□2Fe2++Cl2===2Fe3++2Cl-
②向少量酸性KMnO4溶液中加入FeCl2溶液,若溶液紫红色褪去,证明Fe2+具有还原性
反应原理:□MnO+5Fe2++8H+===5Fe3++Mn2++4H2O
2.铁盐(1)特性:含有Fe3+的盐溶液遇到□SCN-时变成红色
(2)氧化性:含Fe3+的溶液呈□棕黄色,Fe3+具有较强的氧化性
①向FeCl3溶液中滴入几滴KSCN溶液,再加入过量活泼金属(如Fe),若溶液红色褪去,证明Fe3+具有氧化性
反应原理:□2Fe3++Fe===3Fe2+
②向FeCl3溶液中加