第三节铁及其化合物最新考纲:1
掌握铁及其重要化合物的主要性质
掌握铁及其重要化合物的应用
了解常见金属及其重要化合物的制备方法
核心素养:1
宏观辨识与微观探析:认识铁及其化合物的性质,能以Fe2+、Fe3+的相互转化为例,理解变价金属元素的氧化还原反应实质
科学探究与创新意识:能发现和提出有探究价值的氢氧化亚铁的制备探究方案,进行实验探究
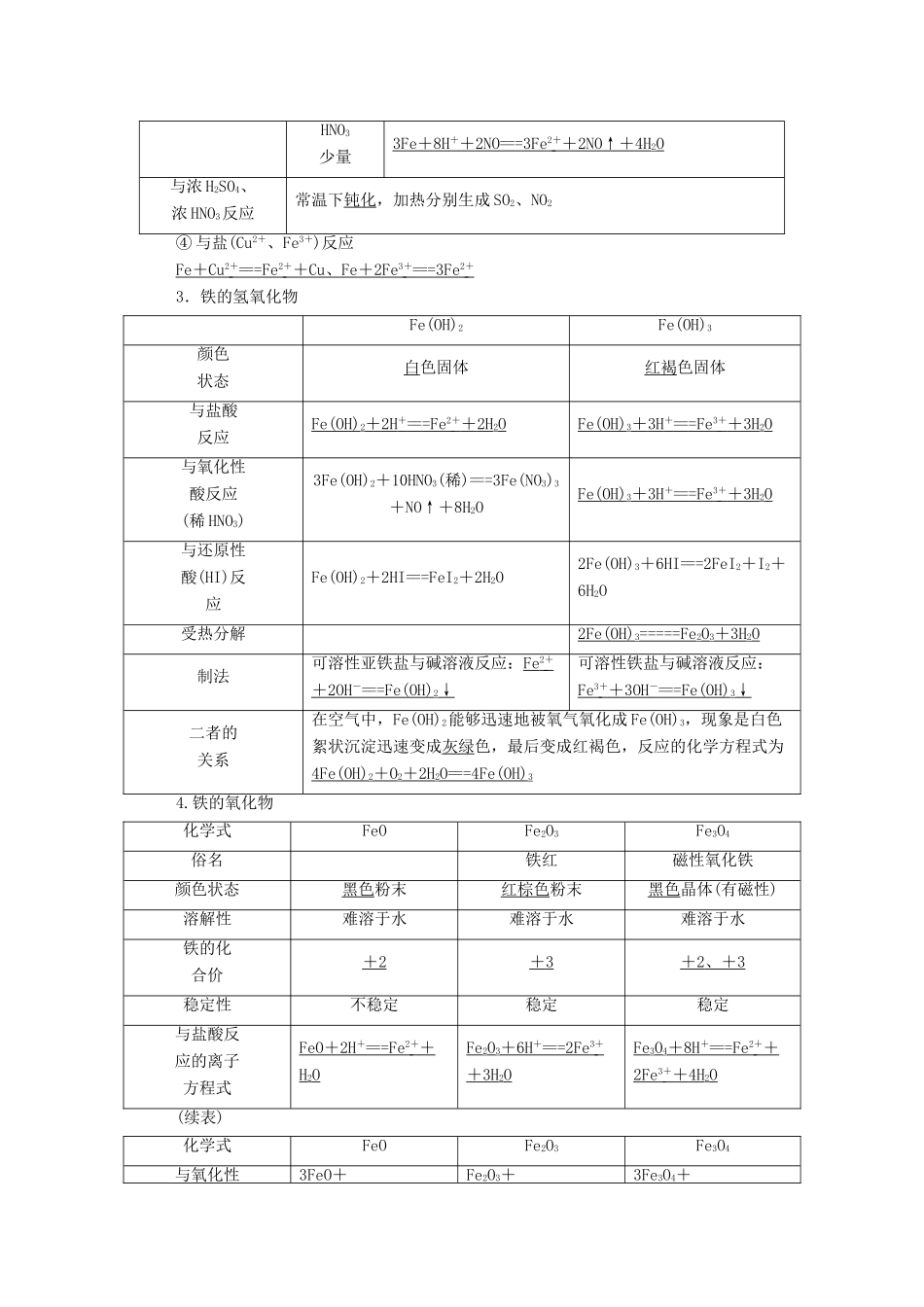
知识点一铁及其氧化物、氢氧化物1.铁的存在2.铁的性质(1)物理性质颜色状态导电、导热性、延展性特性地壳含量银白色固体良好被磁铁吸引占第4位(2)化学性质(写出化学方程式或离子方程式)①与非金属反应与O2反应常温铁锈(成分为Fe2O3·xH2O)点燃3Fe+2O2=====Fe3O4与Cl2反应点燃2Fe+3Cl2=====2FeCl3与S、I2反应Fe+S=====FeS、Fe+I2=====FeI2②与H2O(g)反应3Fe+4H2O(g)=====Fe3O4+4H2③与酸反应与H+反应Fe+2H+===Fe2++H2↑与稀HNO3反应HNO3过量Fe+4H++NO===Fe3++NO↑+2H2OHNO3少量3Fe+8H++2NO===3Fe2++2NO↑+4H2O与浓H2SO4、浓HNO3反应常温下钝化,加热分别生成SO2、NO2④与盐(Cu2+、Fe3+)反应Fe+Cu2+===Fe2++Cu、Fe+2Fe3+===3Fe2+3.铁的氢氧化物Fe(OH)2Fe(OH)3颜色状态白色固体红褐色固体与盐酸反应Fe(OH)2+2H+===Fe2++2H2OFe(OH)3+3H+===Fe3++3H2O与氧化性酸反应(稀HNO3)3Fe(OH)2+10HNO3(稀)===3Fe(NO3)3+NO↑+8H2OFe(OH)3+3H+===Fe3++3H2O与还原性酸(HI)反应Fe(OH)2+2HI===FeI2+2H2O2F