第1节化学反应的方向发展目标体系构建1
通过对日常生活中自发进行的过程的认知,知道化学反应是有方向的,知道化学反应的方向与反应的焓变和熵变有关
2.认识焓判据和熵判据的局限性,会用ΔH-TΔS判断反应正向自发进行的趋势
一、反应焓变与反应方向1.自发过程与自发反应自发过程自发反应含义在一定条件下,不借助外部力量就能自发进行的过程在给定的条件下,可以自发进行到显著程度的化学反应特征具有方向性,即过程的某个方向在一定条件下自发进行,而该过程逆方向在该条件下肯定不能自发进行举例高山流水,自由落体,冰雪融化钢铁生锈应用(1)可被用来完成有用功
如H2燃烧可设计成原电池(2)非自发过程要想发生,必须对它做功
如通电将水分解为H2和O22.反应焓变与反应方向的关系(1)多数能自发进行的化学反应是ΔH0的反应也能自发进行
(3)不能仅用反应焓变来判断反应能否自发进行
二、反应熵变与反应方向1.熵(1)概念:描述体系无序程度的一个物理量,符号为S,单位是J·mol-1·K-1
(2)特点:体系无序程度越大,体系的熵值就越大
(3)影响因素①同一物质:S(高温)>S(低温),S(g)>S(l)>S(s)
②不同物质:相同条件下不同物质具有不同的熵值,分子结构越复杂,熵值越大
③S(混合物)>S(纯净物)
2.反应熵变3.反应熵变与反应方向(1)二者关系(2)结论:不能仅用反应熵变来判断反应能否自发进行
微点拨:熵变正负的判断(1)物质由固态到液态、由液态到气态或由固态到气态的过程,熵变为正值,是熵增加的过程
(2)气体体积增大的反应,熵变通常都是正值,是熵增加的反应
(3)气体体积减小的反应,熵变通常都是负值,是熵减小的反应
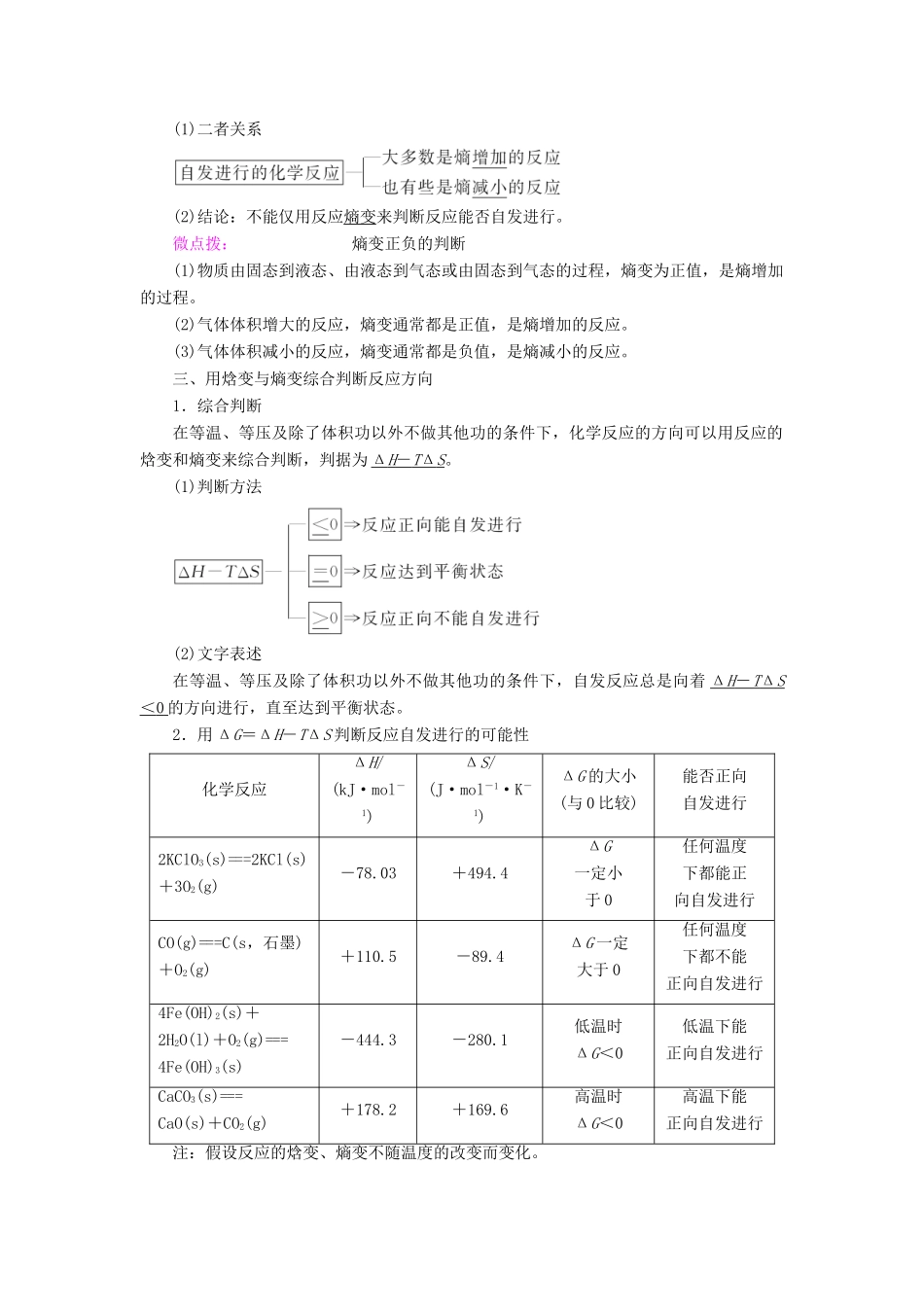
三、用焓变与熵变综合判断反应方向1.综合判断在等温、等压及除了体积功以外不做其他功的条件下,化学反应的方向可以用反应的焓变和熵变来综合判断,判据为ΔH-TΔS