化学反应与能量变化明考纲1.了解化学反应中能量转化的原因,能说出常见的能量转化形式
2.了解化学能与热能的相互转化,了解吸热反应、放热反应、反应热等概念
3.了解焓变与反应热的含义
了解ΔH=H(反应产物)-H(反应物)表达的含义
4.了解热化学方程式的含义
析考情通过对近几年高考题的研究发现,高考对本节内容的考查,主要体现在三个方面:一是以图表为命题背景考查反应物、生成物具有的总能量、化学键键能、正逆反应的活化能的关系及简单计算;二是常见的吸热反应与放热反应的判断;三是热化学方程式的书写及正误判断,题型以选择题、填空题为主,难度不大
考点焓变与反应热1.化学反应中的能量变化(1)化学反应的实质:反应物化学键断裂和生成物化学键形成
其中旧键断裂要吸收能量,新键形成会释放能量
(2)化学反应的特征:既有物质变化,又有能量变化
(3)化学反应中的能量转化形式:热能、光能和电能等,通常主要表现为热能的变化
2.焓变、反应热(1)焓(H):用于描述物质所具有能量的物理量
(2)焓变(ΔH):ΔH=H(生成物)-H(反应物)
单位kJ/mol或kJ·mol-1
(3)反应热:指当化学反应在一定温度下进行时,反应所放出或吸收的热量,通常用符号Q表示,单位kJ/mol或kJ·mol-1
(4)焓变与反应热的关系:对于等压条件下进行的化学反应,如果反应中物质的能量变化全部转化为热能,则有如下关系:ΔH=Qp
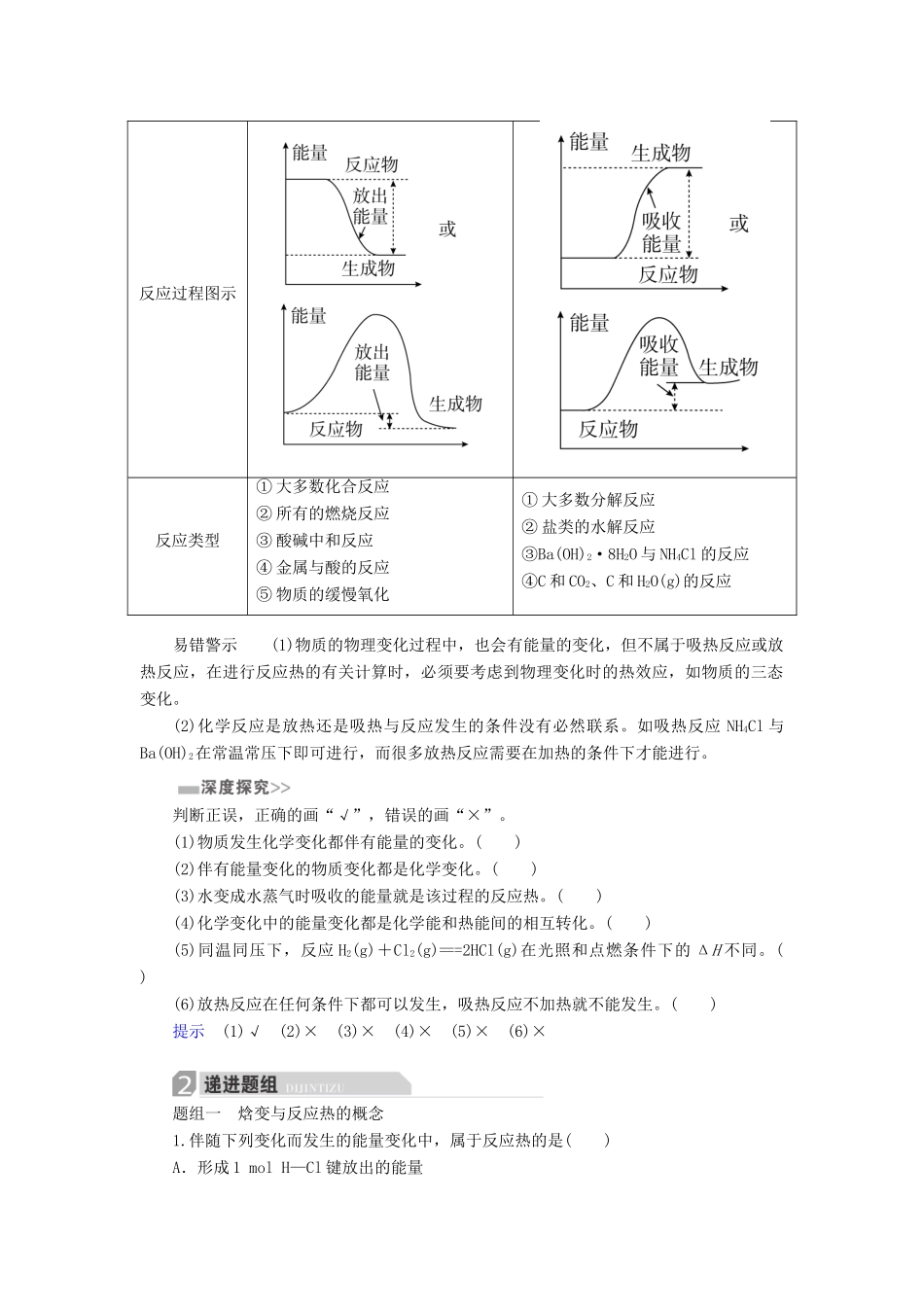
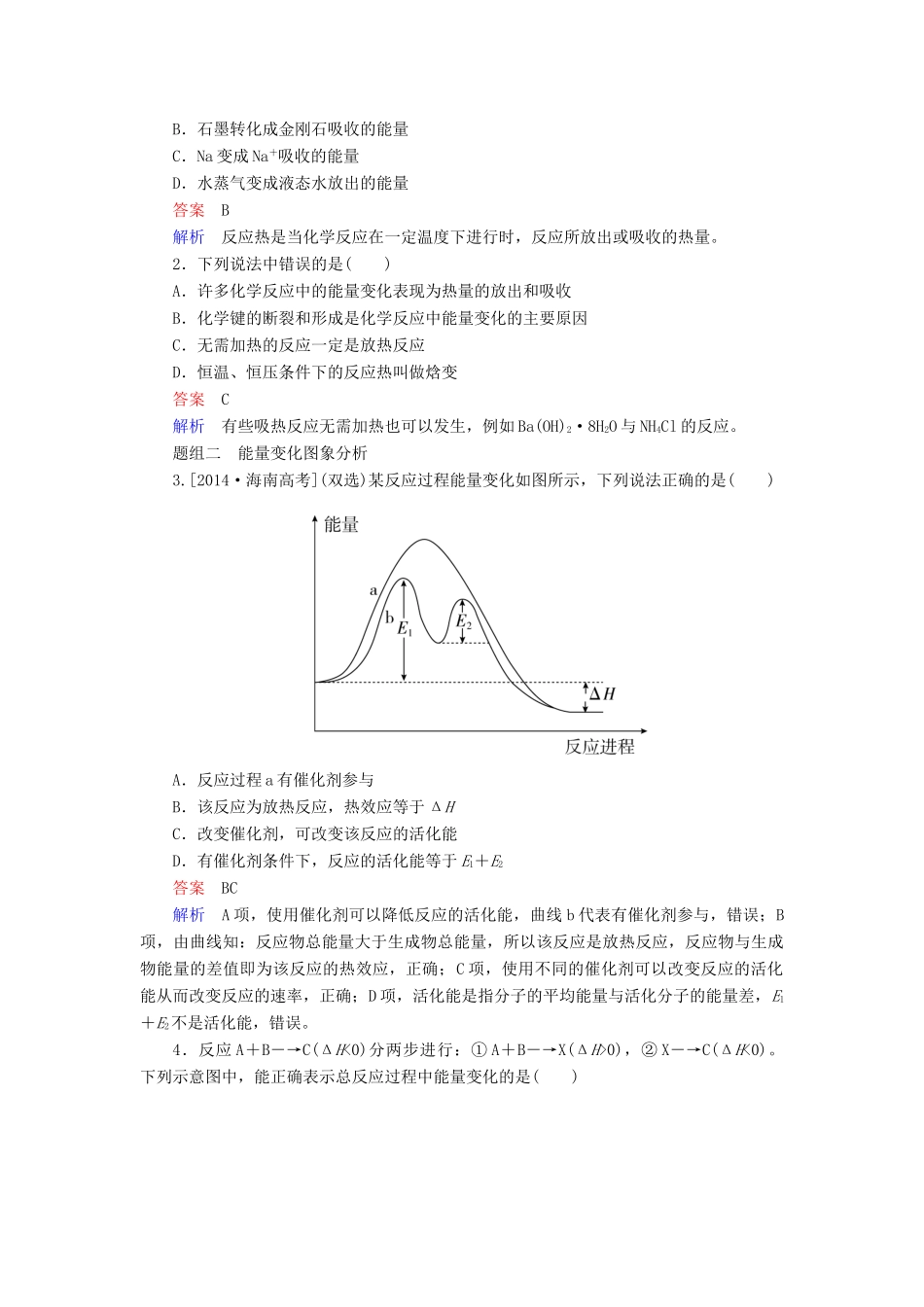
3.吸热反应和放热反应判断依据放热反应吸热反应反应物总能量与生成物总能量的相对大小E反应物>E生成物E反应物