第二节水的电离和溶液的酸碱性第1课时水的电离溶液的酸碱性1
掌握水的离子积Kw和pH的概念
掌握酸、碱对水的电离的影响
3.掌握溶液酸碱性的特征与pH的关系
知识点一水的电离阅读教材P45~P46,思考并填空
1.水的电离水是一种极弱的电解质,电离方程式为H2O+H2OH3O++OH-,简写为H2OH++OH-,水的电离常数K电离=
2.水的离子积常数(1)推导由精确的实验可知,25℃时1L纯水(55
6mol)只有1×10-7molH2O电离,则c(H2O)几乎不变,可视为常数,又因为K电离为常数,所以c(H+)·c(OH-)=K电离·c(H2O)为一常数,记为Kw
(2)表达式Kw=c(H+)·c(OH-)
25℃时,Kw=1
0×10-14
(3)影响因素水的离子积Kw只受温度的影响,温度升高,Kw增大
(4)适用范围Kw不仅适用于纯水,还适用于稀的电解质水溶液
1.判断正误(1)水是电解质,所以纯水能导电
()(2)盐酸中无OH-,只有H+和Cl-以及水分子
()(3)加热,水的电离程度增大,但Kw不变
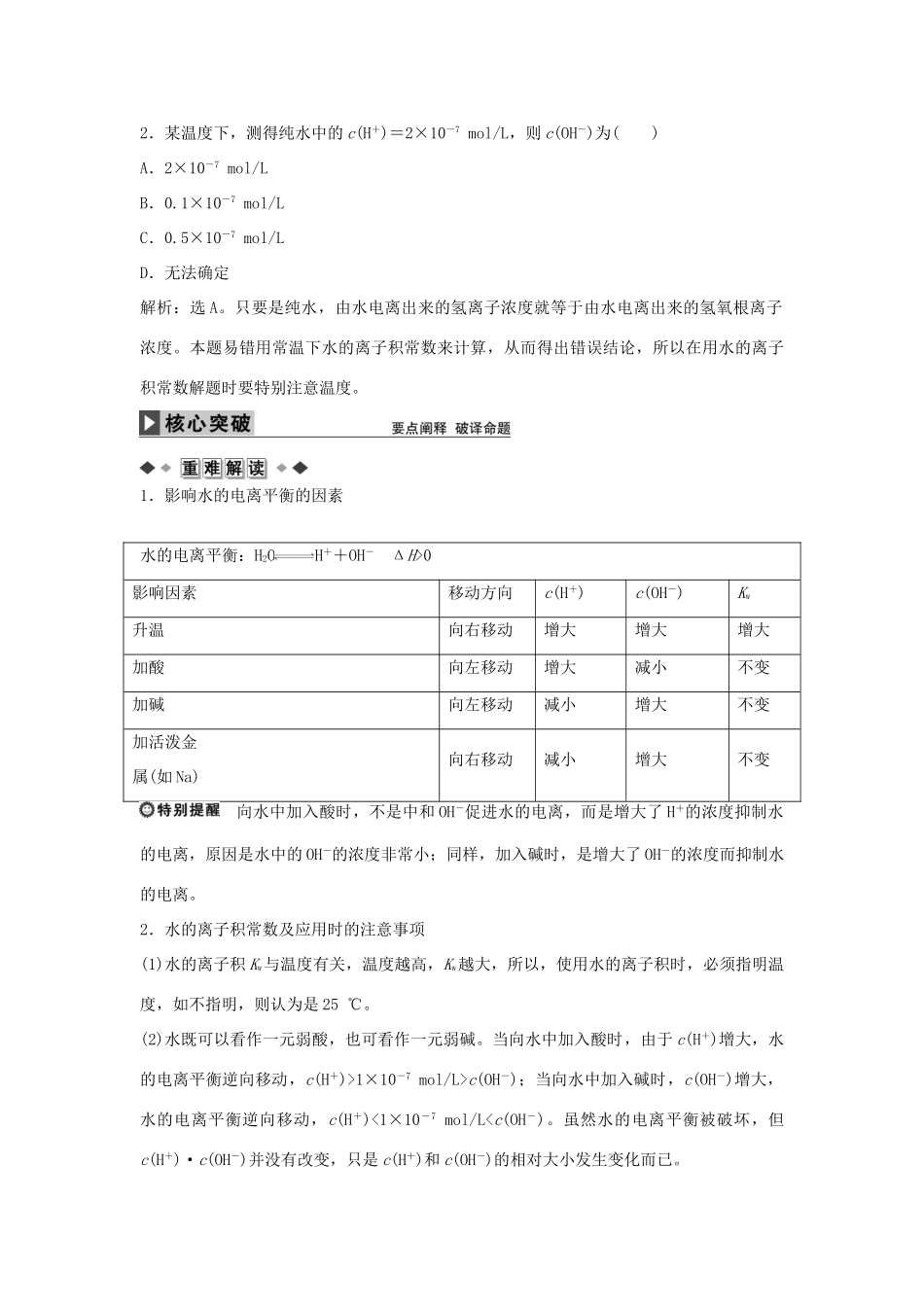
()答案:(1)×(2)×(3)×2.某温度下,测得纯水中的c(H+)=2×10-7mol/L,则c(OH-)为()A.2×10-7mol/LB.0
1×10-7mol/LC.0
5×10-7mol/LD.无法确定解析:选A
只要是纯水,由水电离出来的氢离子浓度就等于由水电离出来的氢氧根离子浓度
本题易错用常温下水的离子积常数来计算,从而得出错误结论,所以在用水的离子积常数解题时要特别注意温度
1.影响水的电离平衡的因素水的电离平衡:H2OH++OH-ΔH>0影响因素移动方向c(H+)c(OH-)Kw升温向右移动增大增大增大加酸向左移动增大减小不变加碱向左移动减小增大不变加活泼金属(如Na)向右移动减小增大不变向水中加入酸时,不是中和OH-促进水的电离,而是增大