第3课时酸碱中和滴定[学习目标定位]1
了解酸碱中和滴定的原理,熟记酸碱中和滴定的主要仪器的名称及用途
掌握酸碱中和滴定的实验操作、计算方法和误差分析
一酸碱中和滴定1
室温下,将pH=12的NaOH溶液分别与等体积的下列酸溶液混合,判断其酸碱性,计算pH,填写下表:酸溶液混合溶液的酸碱性pHpH=2的盐酸中性70
015mol·L-1的硫酸酸性20
004mol·L-1的硫酸碱性112
中和滴定的原理(1)酸碱中和反应的实质可用离子方程式H++OH-===H2O来表示,在中和反应中,H+、OH-之间的物质的量关系是n(H+)=n(OH-);若用参加反应的c(H+)、c(OH-)来表示,其关系式为c(H+)·V酸=c(OH-)·V碱,由此可计算c(H+),其表达式是c(H+)=;也可计算c(OH-),其表达式是c(OH-)=
由c(H+)、c(OH-)可分别求出相应酸、碱的浓度
1032mol·L-1的盐酸溶液,中和25
00mL未知浓度的NaOH溶液,中和完成后用去盐酸27
84mL,请根据上述关系式计算NaOH溶液的物质的量浓度是0
1149mol·L-1
(3)请根据以上原理分析,归纳总结中和滴定的概念是利用中和反应,用已知浓度的酸(或碱)来测定未知浓度的碱(或酸)的实验方法
其中已知浓度的酸(或碱)溶液常称为标准液,未知浓度的碱(或酸)溶液常称为待测液
(4)中和滴定的关键是准确判断滴定终点(中和反应恰好反应完全的时刻),其方法是在待测液中加2~3滴指示剂,观察滴定过程中其颜色的变化,常选用的指示剂是酚酞或甲基橙,不用石蕊溶液的原因是石蕊溶液颜色变化不明显且突变范围太宽
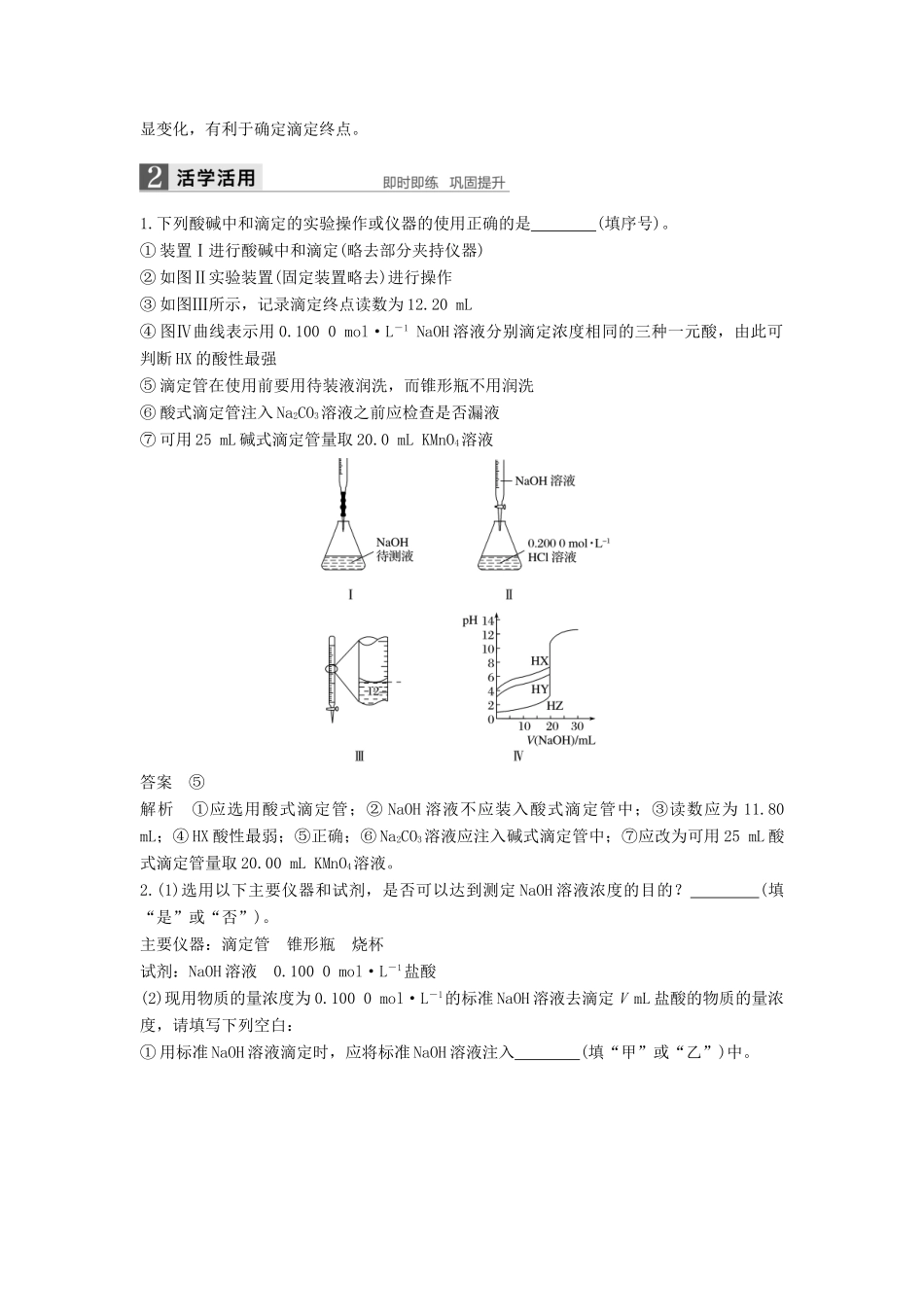
主要仪器及使用酸碱中和滴定所用的主要仪器是锥形瓶和滴定管
(1)滴定管分为两种:①酸式滴定管:包括玻璃活塞、长玻璃管,可盛放酸性溶液、强氧化性溶液,不能盛放碱性溶液及氢氟酸