炔烃【学习目标】1、了解炔烃的物理性质及其变化规律与分子中碳原子数目的关系;2、能以典型代表物为例,理解炔烃的组成、结构和主要化学性质;3、掌握乙炔的实验室制法;4、了解脂肪烃的来源和用途
【要点梳理】要点一、炔烃分子里含有碳碳三键的一类脂肪烃称为炔烃,其分子式的通式可表示为CnH2n-2(n≥2,且为正整数),其中碳原子数小于或等于4的炔烃是气态炔烃,最简单的炔烃是乙炔
1.乙炔的分子组成和结构分子式结构式结构简式空间结构C2H2H—C≡C—HHC≡CH直线形(四个原子处在同一条直线上)2.乙炔的物理性质乙炔是一种无色、无味的气体,密度比空气略小,微溶于水,易溶于有机溶剂
乙炔常因混有杂质而带有特殊难闻的臭味
【高清课堂:炔烃和气态烃燃烧#化学性质】3.乙炔的化学性质(1)乙炔的氧化反应①使酸性高锰酸钾溶液褪色②乙炔的可燃性2C2H2+5O24CO2+2H2O注意:①CH4、C2H4、C2H2三种气体燃烧时,火焰越来越明亮,但黑烟越来越浓,原因是碳的质量分数越来越大
②氧炔焰温度可达3000℃以上,可用氧炔焰来焊接或切割金属
(2)乙炔的加成反应乙炔可与H2、HX、X2(卤素单质)、H2O等发生加成反应
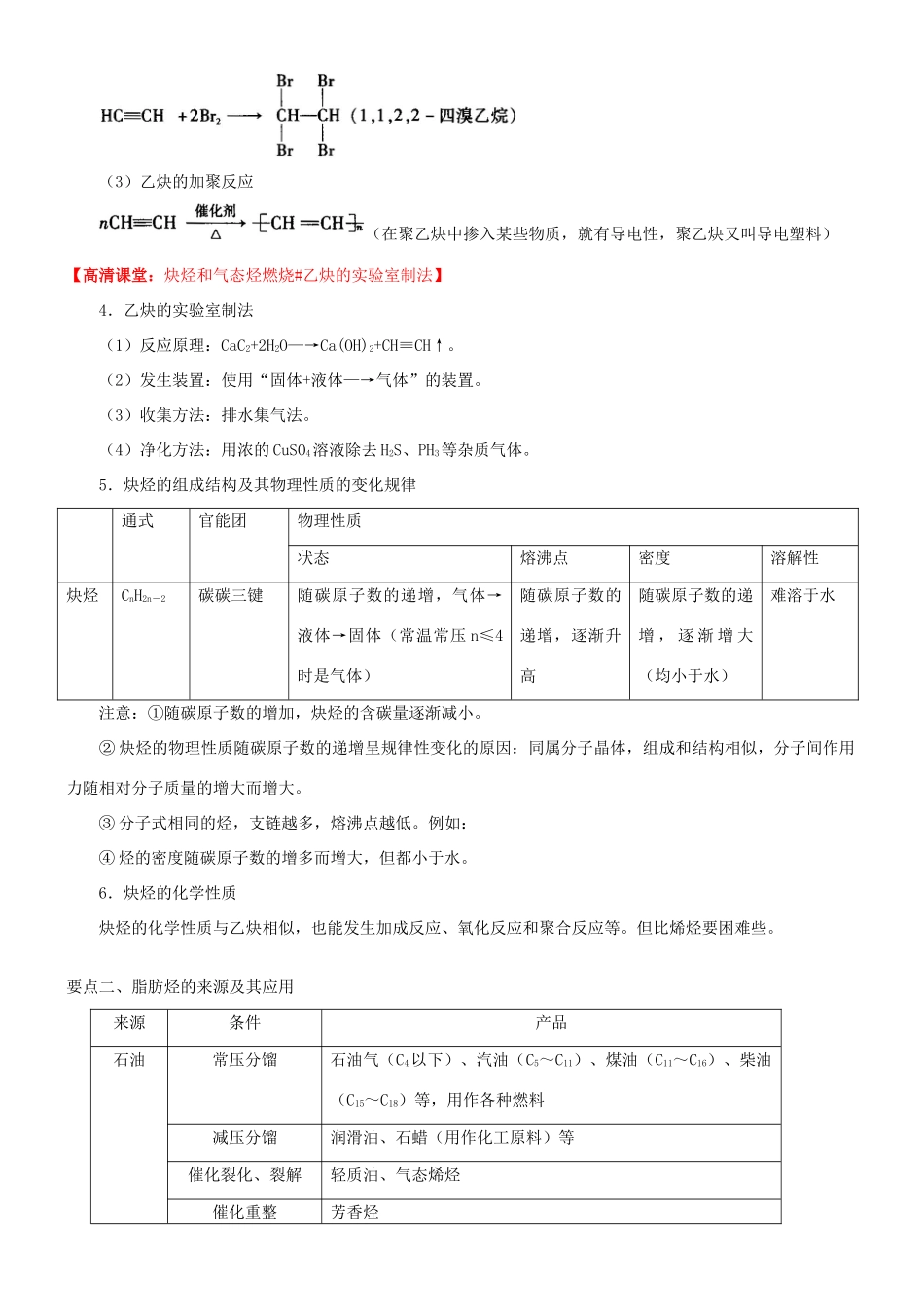
如:HC≡CH+2H2CH3CH3HC≡CH+H2OCH3CHO(3)乙炔的加聚反应(在聚乙炔中掺入某些物质,就有导电性,聚乙炔又叫导电塑料)【高清课堂:炔烃和气态烃燃烧#乙炔的实验室制法】4.乙炔的实验室制法(1)反应原理:CaC2+2H2O—→Ca(OH)2+CH≡CH↑
(2)发生装置:使用“固体+液体—→气体”的装置
(3)收集方法:排水集气法
(4)净化方法:用浓的CuSO4溶液除去H2S、PH3等杂质气体
5.炔烃的组成结构及其物理性质的变化规律通式官能团物理性质状态熔沸点密度溶解性炔烃CnH2n-2碳碳三键随碳原子数的递增,气体→液体→固体(常温常压n≤4时