可逆反应与化学平衡状态题目可逆反应与化学平衡状态第1课时学习目标1
了解化学反应的可逆性,了解可逆反应的概念
通过化学平衡状态的建立过程,知道化学平衡是一种动态的平衡
能根据化学平衡状态的特征,判断化学平衡状态的标志
学习疑问学习建议【预学能掌握的内容】一、可逆反应1.概念在下,既能向方向进行,同时又能向方向进行的反应
如:N2+3H22NH3
2.特点(1)同一条件下,正反应和逆反应
(2)反应进行到底,反应物实现完全转化
(3)反应体系中,与化学反应有关的各种物质
(4)反应达到限度时,反应
二、化学平衡状态1
定义:在一定条件下的可逆反应里,当正、逆两个方向的反应速率时,反应体系中所有参加反应的物质的或保持恒定的状态
也就是在给定条件下,反应达到了“”,这种状态称为化学平衡状态,简称为化学平衡
2.化学平衡的特征化学平衡的特征可以概括为逆、等、动、定、变,即:(1)研究的对象是反应
(2)化学平衡的条件是v正和v逆
(3)化学平衡是一种平衡,此时反应并未停止
(4)当可逆反应达到平衡时,各组分的质量(或浓度)为一
高温、高压催化剂(5)若外界条件改变,平衡可能发生,并在新条件下建立新的平衡
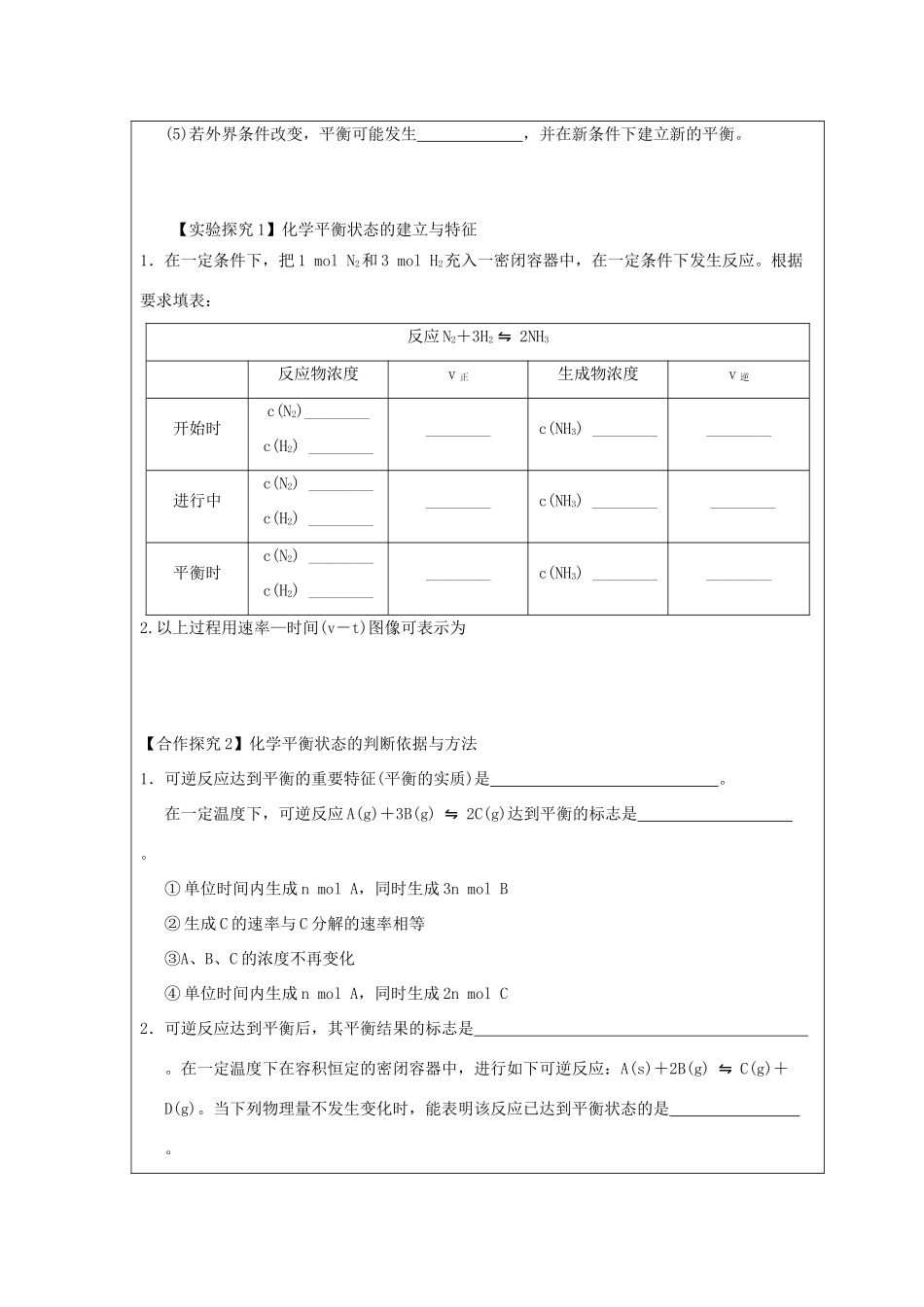
【实验探究1】化学平衡状态的建立与特征1.在一定条件下,把1molN2和3molH2充入一密闭容器中,在一定条件下发生反应
根据要求填表:反应N2+3H2⇋2NH3反应物浓度v正生成物浓度v逆开始时c(N2)________c(H2)________________c(NH3)________________进行中c(N2)________c(H2)________________c(NH3)________________平衡时c(N2)________c(H2)________________c(NH3)________________2
以上过程用速率—时间(v-t)